2025年已接近尾聲。回顧這一年,全球在干細胞治療漸凍癥領(lǐng)域的探索正在持續(xù)推進。從基礎(chǔ)機制研究的不斷深化,到多項臨床研究數(shù)據(jù)的更新,再到各國對細胞治療監(jiān)管框架的逐步完善,干細胞療法正逐漸從概念驗證階段,走向更加規(guī)范、理性的臨床評估階段。
長期以來,漸凍癥因運動神經(jīng)元進行性、不可逆死亡,被認為幾乎不存在“修復(fù)”的可能。但近年來的研究顯示,干細胞并非簡單替代神經(jīng)細胞,而是通過神經(jīng)保護、免疫調(diào)節(jié)和微環(huán)境改善等多重機制,在延緩疾病進展、穩(wěn)定功能狀態(tài)方面展現(xiàn)出一定潛力,為這一高度致殘性疾病提供了新的研究方向。
本文將從2025年全球干細胞治療漸凍癥的基礎(chǔ)研究進展以及臨床研究現(xiàn)狀等方面進行系統(tǒng)梳理,力求為漸凍癥患者及家屬呈現(xiàn)一份清晰、客觀、可參考的年度進展解答。

2025干細胞治療漸凍癥走到哪一步了?從基礎(chǔ)研究到臨床突破的全面解答
一、基礎(chǔ)研究的深度革新:從“是否可行”到“如何更精準(zhǔn)、更可控”
進入2025年,干細胞治療漸凍癥(ALS)的基礎(chǔ)研究,已經(jīng)明顯走出早期“概念驗證”階段,研究重心開始轉(zhuǎn)向機制拆解、路徑優(yōu)化與臨床可轉(zhuǎn)化性提升。
與中風(fēng)等急性腦損傷不同,漸凍癥是一種進行性、系統(tǒng)性神經(jīng)退行性疾病。因此,基礎(chǔ)研究的目標(biāo)并非簡單“修復(fù)缺損”,而是圍繞三個核心問題展開:干細胞究竟通過什么機制延緩運動神經(jīng)元死亡?哪些技術(shù)路徑更安全、更穩(wěn)定?是否存在比整細胞移植更優(yōu)的策略?
025年的突破性進展,主要圍繞以下三個相互關(guān)聯(lián)的方向展開。
1.1 從“細胞替代”轉(zhuǎn)向“神經(jīng)保護”:機制認識更加清晰
早期研究曾希望干細胞能直接替代死亡的運動神經(jīng)元,但現(xiàn)在科學(xué)界已形成共識:在漸凍癥中,干細胞的核心價值在于系統(tǒng)性保護而非直接替換。[1]
近期的動物模型和體外研究證實,干細胞(如間充質(zhì)干細胞MSC)主要通過以下方式發(fā)揮作用:
- 分泌神經(jīng)營養(yǎng)因子,延緩神經(jīng)元死亡。
- 抑制慢性神經(jīng)炎癥,改善有毒的細胞微環(huán)境。
- 改善線粒體功能和抗氧化應(yīng)激,保護神經(jīng)元。
因此,干細胞在疾病中更接近于“系統(tǒng)調(diào)節(jié)器”,而非“神經(jīng)元工廠”。這一關(guān)鍵認識的轉(zhuǎn)變,為臨床試驗設(shè)定了更現(xiàn)實的目標(biāo)——延緩疾病進展、延長穩(wěn)定期。
1.2 研究工具革新:“芯片器官”與iPSC模型帶來人源化精準(zhǔn)研究
對疾病機制的深刻理解,依賴于能模擬人體真實復(fù)雜性的研究工具。傳統(tǒng)靜態(tài)培養(yǎng)和動物模型存在局限,而2025年,兩類前沿技術(shù)正推動研究進入“人源化”和“動態(tài)化”的新范式。
一方面,利用患者細胞構(gòu)建的“芯片上的ALS”模型,在動態(tài)流體中同時培養(yǎng)運動神經(jīng)元與血腦屏障,創(chuàng)造了接近體內(nèi)的“活體”微環(huán)境。這使得科學(xué)家能更真實地觀察病理過程(如谷氨酸興奮性毒性),為高效篩選藥物和評估干細胞療法提供了革命性平臺。[2]
另一方面,誘導(dǎo)多能干細胞(iPSC)技術(shù)已成熟應(yīng)用于基礎(chǔ)研究。利用患者來源的iPSC分化出運動神經(jīng)元,能精準(zhǔn)模擬不同遺傳亞型的早期病理,用于測試干細胞分泌因子的真實效果或篩選協(xié)同藥物組合。這類研究揭示了一個關(guān)鍵發(fā)現(xiàn):不同亞型的漸凍癥對同一干預(yù)策略的反應(yīng)存在顯著差異。[3]
1.3 未來方向:從機制到精準(zhǔn)醫(yī)療
上述工具與發(fā)現(xiàn)的結(jié)合,正將基礎(chǔ)研究的方向從籠統(tǒng)的“是否有效”,推向更具針對性的“對誰、在何時、以何種方式最有效”。這為未來實現(xiàn)臨床分層治療和個體化精準(zhǔn)醫(yī)療方案奠定了堅實的科學(xué)基礎(chǔ)。
總而言之,2025年的基礎(chǔ)研究正通過厘清核心機制、革新研究工具,系統(tǒng)性地破解干細胞治療漸凍癥在精準(zhǔn)性與可控性上的難題,為后續(xù)的臨床轉(zhuǎn)化鋪平道路。
二、臨床進展:多點突破,證據(jù)日益堅實
2025年,干細胞治療漸凍癥(ALS)的臨床研究已從實驗室走向病床,取得了多項具有里程碑意義的進展。多條主流技術(shù)路徑均已看到效果。
1. 美國(間充質(zhì)干細胞路徑):NurOwn?沖刺最終驗證
2025年4月10日,BrainStorm Cell Therapeutics宣布向美國食品藥品監(jiān)督管理局(FDA)提交了NurOwn??的新藥臨床試驗(IND)修正案。[4]
NurOwn? 是該公司開發(fā)用于治療肌萎縮側(cè)索硬化癥(ALS,又稱漸凍癥)的自體間充質(zhì)干細胞療法。這一重要里程碑為該公司備受期待的3b期臨床試驗的啟動奠定了基礎(chǔ),該試驗是根據(jù)特殊方案評估(SPA)與FDA合作設(shè)計的。

這場即將打響的3b期臨床試驗,規(guī)模宏大,預(yù)計將招募約200名ALS患者,并分兩個階段有序推進。
在A部分,患者們將進入24周的雙盲試驗期,在此期間,他們會被隨機分為兩組,一組接受三劑NurOwn治療,另一組則使用安慰劑。如此設(shè)計,能最大程度減少主觀因素干擾,精準(zhǔn)檢驗NurOwn的真實療效。而試驗的主要療效終點,便是聚焦從基線到第24周的ALSFRS – R評分變化,通過對比NurOwn組和安慰劑組,清晰洞察病情進展差異。
待A部分結(jié)束,所有參與者,包括起初使用安慰劑的患者,都將迎來新的希望 —— 進入開放標(biāo)簽擴展試驗(B部分)。在接下來的24周里,他們都有機會接受三劑NurOwn治療,進一步探索該療法長期干預(yù)的效果。并且,一旦A部分取得成功,BrainStorm就可提交生物制品許可申請(BLA),大大加快NurOwn獲得批準(zhǔn)上市的進程,讓患者早日受益。
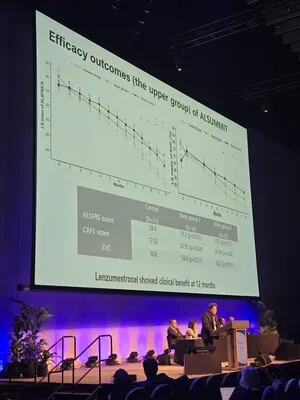
2.韓國(神經(jīng)細胞路徑):Neuronata-R?明確獲益
韓國Corestemchemon公司開發(fā)的干細胞療法Neuronata-R?(lenzumestrocel)在2025年取得了關(guān)鍵臨床進展。[5]
該療法的III期臨床試驗結(jié)果顯示,其核心價值在于為特定亞組的患者帶來了明確獲益。盡管未在所有入組患者中達到主要終點,但對病情進展相對緩慢的患者群體進行分析時,發(fā)現(xiàn)了具有統(tǒng)計學(xué)意義的療效。
與服用安慰劑的患者相比,接受治療的患者在12個月后,其運動功能評分(ALSFRS-R)和呼吸功能指標(biāo)(慢肺活量)都維持得更好。同時,患者血液中標(biāo)志神經(jīng)損傷的“神經(jīng)絲輕鏈蛋白”水平也顯著降低,從生物學(xué)上證實了該療法的神經(jīng)保護作用。
這些發(fā)現(xiàn)具有重要意義,它們不僅證明了Neuronata-R?有潛力延緩特定患者的病情進展,更重要的是為漸凍癥的“精準(zhǔn)分層治療” 提供了切實依據(jù)。基于這些積極數(shù)據(jù),公司計劃在2025年內(nèi)與美國FDA進行溝通,并尋求加速審批路徑,以期早日讓該療法服務(wù)于合適的患者。
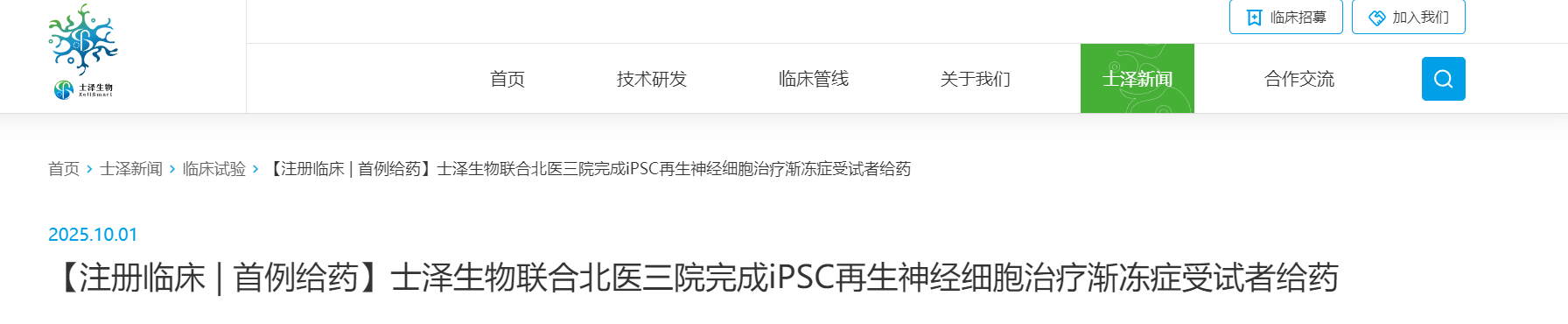
3.中國(iPSC前沿路徑):XS228注射液實現(xiàn)“雙報雙批”里程碑
2025年由中國企業(yè)士澤生物研發(fā)的全球首款“現(xiàn)貨型”異體iPSC衍生神經(jīng)前體細胞新藥——XS228細胞注射液,在2025年先后獲得了美國FDA和中國NMPA的完全批準(zhǔn),實現(xiàn)了“中美雙報雙批”的里程碑。[6]
同年9月,該藥在北京大學(xué)第三醫(yī)院完成了全球首例受試者給藥,正式啟動注冊臨床試驗。這款療法利用可規(guī)模化生產(chǎn)的通用型細胞,旨在為患者中樞神經(jīng)系統(tǒng)補充健康的神經(jīng)前體細胞,代表了干細胞再生醫(yī)學(xué)治療神經(jīng)退行性疾病的前沿探索。
4.日本(傳統(tǒng)細胞路徑):STR03開展II期對照研究
在日本,一項更為傳統(tǒng)的細胞療法研究也正按計劃推進。2025年7月,Nipro公司與札幌醫(yī)科大學(xué)合作,正在開展一項使用自體骨髓間充質(zhì)干細胞(STR03)?的II期臨床試驗。[7]
這項研究采用雙盲、隨機、安慰劑對照設(shè)計,計劃招募106名早期、病情較輕的漸凍癥患者,旨在通過更嚴格的臨床研究,系統(tǒng)評估該療法的安全性與有效性,標(biāo)志著傳統(tǒng)細胞療法向高級別證據(jù)邁出了堅實一步。

2025干細胞治療漸凍癥臨床總結(jié)
綜合2025年全球已披露的臨床研究可以看到,干細胞治療漸凍癥正在呈現(xiàn)出幾個清晰趨勢。
首先,療效評估更加務(wù)實。無論是美國的NurOwn?、韓國的Neuronata-R?,還是中國的XS228注射液,臨床終點均不再以“逆轉(zhuǎn)疾病”為目標(biāo),而是聚焦于延緩功能下降、維持呼吸能力、延長穩(wěn)定期等更符合疾病自然史的指標(biāo)。這一變化,標(biāo)志著該領(lǐng)域已從早期探索階段,進入以臨床真實獲益為導(dǎo)向的成熟評估階段。
其次,患者分層的重要性被反復(fù)驗證。Neuronata-R?在進展較慢患者中的明確獲益,以及多項研究中對早期、呼吸功能較好患者的優(yōu)先入組設(shè)計,表明某些干細胞療法并非“對所有ALS患者同樣有效”,而更可能適用于特定患者。這一認識正在深刻影響臨床試驗設(shè)計和未來的適應(yīng)癥定位。
第三,技術(shù)路線開始分化并各自推進。自體MSC路徑強調(diào)安全性與規(guī)范化驗證;神經(jīng)相關(guān)細胞路徑嘗試在神經(jīng)保護基礎(chǔ)上實現(xiàn)功能維持;iPSC衍生細胞則代表更前沿的再生醫(yī)學(xué)探索。多條路線并行發(fā)展,使該領(lǐng)域避免了“單一技術(shù)失敗即整體停滯”的風(fēng)險。
總體而言,2025年的臨床證據(jù)尚不足以支撐“治愈漸凍癥”的結(jié)論,但已明確證明:在合適人群中,干細胞療法具備可重復(fù)的生物學(xué)效應(yīng)和臨床潛力。
未來展望
基于2025年的突破,未來幾年該領(lǐng)域的發(fā)展將聚焦于以下幾個關(guān)鍵方向:
1.聯(lián)合療法的探索:鑒于漸凍癥病理機制的復(fù)雜性,單一干細胞療法可能效力有限。未來的趨勢是將干細胞(提供神經(jīng)保護與微環(huán)境支持)與靶向特定致病環(huán)節(jié)的基因療法(如針對SOD1、C9orf72基因的反義寡核苷酸)或小分子藥物聯(lián)合使用,形成“雞尾酒”式治療方案,從多通路協(xié)同遏制疾病進展。
2.監(jiān)管與可及性路徑的完善:隨著更多臨床數(shù)據(jù)的積累,全球藥品監(jiān)管機構(gòu)將加速完善針對干細胞等先進療體細胞治療產(chǎn)品的審評指南。如何平衡加速審批以惠及患者與確保長期安全有效的證據(jù),將是監(jiān)管科學(xué)的核心議題。同時,“現(xiàn)貨型”通用細胞產(chǎn)品的研發(fā)成功,是解決個性化細胞療法成本高昂、制備周期長等可及性瓶頸的關(guān)鍵。
3.個體化與精準(zhǔn)醫(yī)療的深化:利用iPSC模型、血液神經(jīng)絲輕鏈蛋白等生物標(biāo)志物,未來有望在治療前預(yù)測患者對特定干細胞療法的反應(yīng)。臨床實踐將走向?“分層治療”?:根據(jù)患者的基因型、疾病進展速度、免疫狀態(tài)等特征,匹配最優(yōu)的細胞類型、給藥時機和聯(lián)合策略。
結(jié)語
2025年,對于關(guān)注漸凍癥治療的人們而言,是充滿實質(zhì)性訊號的一年。基礎(chǔ)研究揭示了干細胞并非簡單的“替代工”,而是更接近于“調(diào)節(jié)者”與“支持者”,這一認知革命讓治療策略變得更加精細和務(wù)實。臨床研究則從早期的安全性報告,邁入了嚴謹驗證療效、甚至探索精準(zhǔn)分層的新階段,全球多項試驗傳來了積極的進展。
盡管目前仍沒有任何一款干細胞療法被正式批準(zhǔn)為漸凍癥的標(biāo)準(zhǔn)治療,但路徑已經(jīng)清晰,步伐正在加快。科學(xué)的嚴謹性要求我們必須保持耐心與理性,認識到從臨床驗證到成功上市仍有關(guān)山需越。然而,這些持續(xù)取得的突破,無疑為全球數(shù)十萬漸凍癥患者及家庭帶來了前所未有的希望之光——那束光,正在從實驗室和臨床研究中心,越來越清晰地照向未來。
這不是終點,而是一個更富希望的新起點。
參考資料:
[1]https://pmc.ncbi.nlm.nih.gov/articles/PMC12636885/?utm_source=chatgpt.com
[2]http://health.people.com.cn/n1/2025/0625/c14739-40508423.html
[3]https://www.nature.com/articles/s41593-025-02118-7?utm_source=chatgpt.com
[4]https://ir.brainstorm-cell.com/2025-04-10-BrainStorm-Cell-Therapeutics-Submits-IND-Amendment-to-FDA,-Paving-the-Way-for-Phase-3b-Trial-of-NurOwn-R-in-ALS
[5]https://finance.yahoo.com/news/neuronata-r-phase-3-results-022800888.html?guce_referrer=aHR0cHM6Ly93d3cuZ29vZ2xlLmNvbS8&guce_referrer_sig=AQAAALcyn23zsAYAO8iz84Lckrw1zOurjnupKA2sOENs5theIqqpwn6geintd0hiTG8qcg3uQZKmGDS6v3Azk3pDja5LL8X9xqah0xZqAMEdH4tB3uk6lD96pO6cA_mF9TK6sn9p8us0H73h5WQrIxt-HEl4mLsTo4bnC_g00RTrDEWZ&guccounter=2
[6]https://www.xellsmart.com/lcsy/191.html
[7]https://www.nipro.co.jp/assets/document/newsrelease/250724.pdf?utm_source=chatgpt.com
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信