近年來,腎臟疾病已成為威脅全球公共健康的主要疾病之一。根據世界衛生組織《2019年全球健康評估》報告,腎臟疾病已躋身全球十大死因之列,其發病率和死亡率持續攀升,給臨床治療和公共衛生體系帶來嚴峻挑戰。因此,亟需探索更有效的干預策略,以修復受損腎組織、延緩疾病進展。
腎臟疾病本質上是多種細胞結構與功能異常引發的病理綜合征,其核心病理機制涉及腎小球、腎小管及間質細胞的損傷與功能障礙。因此,恢復腎臟功能細胞的數量與活性是治療腎病的關鍵。在此背景下,干細胞作為再生醫學領域的核心研究對象,憑借其多向分化潛能、免疫調節及組織修復能力,為腎臟疾病的治療提供了全新思路。
近年來,干細胞療法在腎病領域的研究與應用取得了顯著進展。干細胞在腎病領域中也越來越受到醫學界重視。目前,干細胞用于糖尿病腎病、狼瘡腎炎已相繼進入我國干細胞備案的臨床階段,并且開展多中心臨床研究方式,提高了臨床試驗的真實有效性。干細胞已逐漸在慢性腎病(CKD)、急性腎損傷(AKI)、糖尿病腎病(DN)、狼瘡性腎炎(LN)等腎臟疾病的基礎研究中表現出良好研究成果,為臨床應用奠定了基礎。
本文基于多項臨床試驗與機制研究,分析不同年齡段干細胞治療腎病的療效特點及影響因素。
不同年齡段接受干細胞治療腎病,療效差異究竟有多大?
一、不同年齡段的生理特點與腎病差異
兒童患者:
- 生理特點:免疫系統未完全成熟,再生能力較強,但易受遺傳性或先天性腎病影響(如先天性腎病綜合征)。
- 腎病類型:多為遺傳性或先天性缺陷,如Alport綜合征、多囊腎。
中青年患者(18-60歲):
- 主要病因:糖尿病腎病(DN)、狼瘡性腎炎(LN)、IgA腎病等免疫相關疾病。
- 治療難點:炎癥反應劇烈,纖維化進程較快。
老年人(>60歲):
- 合并癥復雜:常伴高血壓、糖尿病、心血管疾病,腎功能衰退加速。
- 腎病類型:慢性腎臟病(CKD)3-5期、急性腎損傷(AKI)合并多器官功能不全。
二、不同年齡段的療效差異與臨床證據
1.干細胞療法對兒童腎病綜合征的改善效果:臍血MSCs的安全性與療效
2022年,意大利再生醫學實驗室在行業期刊《干細胞研究與治療》發表了一篇關于《臍血間充質干細胞在耐多藥腎病綜合征患兒中的首次臨床應用》的臨床研究成果。

本研究中,11名接受CB-MSCs治療的患兒(中位年齡為13歲)均未出現嚴重不良反應或腎功能惡化,輸注耐受性良好。
療效方面,3名無基因突變的非遺傳性局灶節段性腎小球硬化癥(SRNS)患者達到部分或完全緩解(蛋白尿降至腎病范圍以下),其中2例緩解持續超過1年并減少免疫抑制劑用量。
其余患者蛋白尿中位值輕微改善。但未緩解患者的腎功能在12個月隨訪期間總體穩定。
綜上所述,間充質干細胞為非遺傳性SRNS患兒提供了安全有效的治療選擇,年輕患者的響應優勢及非遺傳性腎病的療效提示,間充質干細胞可能對年輕腎病兒童(尤其是非遺傳性病例)具有潛在療效。
2.干細胞治療中年慢性腎病患者:療效與年齡相關性
2018年,我國學者開展了一項臨床研究,評估胚胎源性前體干細胞對慢性腎臟病(CKD)的治療潛力,重點考察其延緩腎功能衰竭進展的療效。研究納入CKD 3a期(平均年齡44.2歲)和3b期(平均年齡54.8歲)患者,通過分組對照分析干細胞療法對腎功能指標的改善效果。結果顯示:

3a期患者:78.5%的病例腎功能顯著改善,腎小球濾過率(eGFR)顯著提升,男性患者eGFR達54 mL/min/1.73m2(血清肌酐降至128±0.02 μmol/L),女性患者分別為47 mL/min/1.73m2和113±0.2 μmol/L。
3b期患者:66.7%的病例GFR下降,但治療后未出現腎功能惡化,血清肌酐和腎小管功能呈持續改善趨勢。(見圖1)
年輕患者(3a期)對干細胞治療的響應更顯著,可能與腎臟損傷程度較輕有關。

綜上所述,本研究證實干細胞治療在慢性腎臟病(尤其是年輕患者)中具有顯著療效,能夠逆轉腎功能損傷并實現分期降級,為早期腎病患者提供了新的治療選擇。盡管3b期患者療效有限,但其穩定性和代謝改善趨勢表明干細胞可能作為綜合治療的重要組成部分。
3.老年晚期慢性腎病的干細胞治療分層策略:早期與晚期患者的臨床差異
2023年,尼加拉瓜國研究所在在行業期刊《干細胞移植醫學》上發表了一篇關于《基質血管成分干細胞療法治療原因不明的慢性腎病(中美洲腎病)的安全性》的臨床研究案例。

在這項首次人體開放標簽安全性研究中,納入了18名平均年齡55歲原因不明的慢性腎病 (CKDu)(3-5期)患者進行了36個月的隨訪。研究表明:
所有患者治療前腎功能(eGFR)均顯著下降,晚期患者(4/5期)惡化更明顯。治療后2個月,所有分期患者的eGFR均迅速恢復,且18名患者均出現早期臨床反應,與總細胞劑量無關。
長期療效分層:
- 早期患者(3a/3b期,eGFR初始>30):12個月時改善持續,36個月時進一步穩定或提升(3a期恢復率25.1%,3b期12.4%),且無透析需求;(見圖1)
- 晚期患者(eGFR初始<30):4期患者36個月時腎功能喪失29.2%,其中3人分別在18或36個月需透析,5期患者12個月時全部需透析。
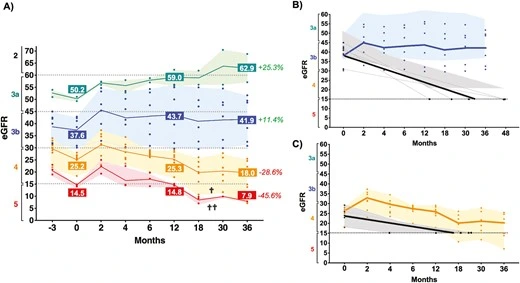
干細胞治療在晚期慢性腎臟病中的療效呈現顯著分層:對早期患者(eGFR>30)可實現功能恢復并避免透析,對晚期患者(eGFR<30)可延緩進展。其非劑量依賴性早期反應和長期分層效應為細胞治療的機制研究與臨床轉化提供了新方向。
4.核心結論:年齡與療效的關聯性
年輕患者:非遺傳性腎病、早期階段(eGFR>30)患者對干細胞響應最佳,可能實現功能恢復或分期降級。
中年晚期患者:干細胞可延緩腎功能惡化,通過修復腎小球損傷、抑制纖維化,實現腎功能分期降級,但需結合其他治療(如免疫抑制劑)。
老年晚期患者:干細胞無法徹底逆轉終末期腎病,但可延緩進展,為透析/移植爭取時間。
三、機制差異:為何不同年齡段療效不同?
1.炎癥與免疫狀態
兒童:免疫系統未成熟,MSCs的免疫調節作用更易發揮,但對自身免疫性疾病(如LN)的療效可能受限。
老年人:慢性炎癥(如TNF-α、IL-6升高)更顯著,MSCs的抗炎作用可顯著改善腎功能,但需更高劑量或聯合抗炎藥物。
2.干細胞歸巢與分化能力
中青年:干細胞歸巢至損傷部位的效率較高,分化為腎小管上皮細胞或內皮細胞的能力更強。
老年人:干細胞衰老(Senescence)導致分化能力下降,需通過預處理(如IL-17A激活)增強其功能。
3.纖維化程度
慢性腎病晚期患者:纖維化已嚴重,MSCs的抗纖維化作用需長期干預(如多次輸注),短期療效可能有限。
未來研究方向與臨床建議
1.分年齡段精準化臨床試驗設計
針對兒童、中青年及老年人群設計獨立臨床試驗,以探索不同生命周期階段的最優治療方案。兒童患者將聚焦于臍帶間充質干細胞(UC-MSCs)的使用,結合基因編輯技術(如CRISPR)增強其抗纖維化能力,以匹配兒童腎臟修復潛力強、免疫系統未成熟的生理特點;中青年患者將通過頭對頭試驗比較靜脈注射、腎動脈導管或腎包膜下注射的療效與安全性;老年人群則需結合小劑量免疫調節劑(如雷帕霉素),通過優化免疫微環境減少干細胞排斥反應,同時增強其抗炎與組織修復功能。此類分層設計可為不同年齡段患者提供個體化治療策略,解決當前干細胞治療“一刀切”模式的異質性問題。
2.優化治療策略與長期隨訪的必要性
為提升干細胞治療的遠期療效與安全性,需同步推進多靶點干預策略與長期隨訪機制:
- 兒童組:基因編輯UC-MSCs可定向增強抗膠原沉積、促進血管再生的基因表達(如TGF-β抑制因子),以阻斷纖維化進程;
- 老年人組:雷帕霉素通過抑制mTOR通路可減少炎癥因子釋放,同時延長MSCs在腎組織的存活時間,平衡療效與副作用;
- 隨訪優化:當前研究多聚焦短期(<1年)指標,但干細胞治療的持久性需通過3-5年隨訪驗證,重點關注eGFR穩定性、蛋白尿復發率及遠期并發癥(如腫瘤風險或免疫異常),為臨床轉化提供可靠證據。
相關閱讀:干細胞療法能否為腎病帶來長期改善?718例患者揭示真相
結語
干細胞治療腎病的療效存在顯著年齡差異:兒童短期修復能力強但需關注長期發育影響,中青年需重點控制慢性炎癥,老年患者需優化細胞活性與聯合治療。未來需通過分年齡段研究、優化給藥方案及多學科協作,最大化干細胞治療的個體化療效,為全年齡段腎病患者帶來希望。
參考資料:
https://fctiinc.com/wp-content/uploads/2018/11/04-Efficacy-of-renal-precursor-stem-cells-in-management-of-chronic-kidney-disease-CN.pdf
Michael H Carstens, Nelson García, Sreedhar Mandayam, Biruh Workeneh, Indiana Pastora, Carlos Calderón, Kenneth A Bertram, Diego Correa, Safety of Stromal Vascular Fraction Cell Therapy for Chronic Kidney Disease of Unknown Cause (Mesoamerican Nephropathy), Stem Cells Translational Medicine, Volume 12, Issue 1, January 2023, Pages 7–16, https://doi.org/10.1093/stcltm/szac080
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信