阿爾茨海默病(AD)存在巨大的未滿足醫(yī)療需求,目前尚無(wú)有效的治療方案。現(xiàn)有的藥物治療僅能緩解癥狀,無(wú)法阻止持續(xù)的神經(jīng)退行性變。間充質(zhì)干細(xì)胞(MSCs)療法因其治療AD的潛力而受到廣泛研究,但其療效仍未得到證實(shí)。
干細(xì)胞治療阿爾茨海默病,到底有沒有效?一項(xiàng)基于17項(xiàng)臨床研究的綜述給出了答案
為了證實(shí)間充質(zhì)干細(xì)胞治療阿爾茨海默病的臨床可行性,近日,《組織工程與再生醫(yī)學(xué)》雜志發(fā)表了一篇“間充質(zhì)干細(xì)胞(MSCs)治療阿爾茨海默病療效:臨床結(jié)果綜述”的論文。該研究旨在通過(guò)回顧17項(xiàng)臨床試驗(yàn)和4篇相關(guān)論文來(lái)評(píng)估MSCs對(duì)AD患者的治療效果[1]。

最終對(duì)17項(xiàng)臨床試驗(yàn)和5項(xiàng)相關(guān)臨床結(jié)果的初步分析表明,間充質(zhì)干細(xì)胞治療阿爾茨海默病患者中總體可行且安全,部分患者的認(rèn)知功能或生活質(zhì)量顯示出改善跡象,提示其具有潛在的治療價(jià)值。然而,確切的療效仍需進(jìn)一步驗(yàn)證。
這些臨床探索建立在MSCs多靶點(diǎn)治療潛力的理論基礎(chǔ)之上。與單靶點(diǎn)藥物不同,MSCs被認(rèn)為能通過(guò)多種協(xié)同機(jī)制干預(yù)AD的復(fù)雜病理過(guò)程,這構(gòu)成了其臨床研究的主要依據(jù):
間充質(zhì)干細(xì)胞治療阿爾茨海默病的潛在機(jī)制
間充質(zhì)干細(xì)胞有望通過(guò)多模式作用機(jī)制干預(yù)AD的復(fù)雜病理過(guò)程,這與多數(shù)單靶點(diǎn)藥物形成鮮明對(duì)比,也是其臨床研究的理論基礎(chǔ)。主要機(jī)制包括:
- 神經(jīng)營(yíng)養(yǎng)支持:MSCs分泌腦源性神經(jīng)營(yíng)養(yǎng)因子(BDNF)、膠質(zhì)細(xì)胞系衍生神經(jīng)營(yíng)養(yǎng)因子(GDNF)等多種因子,促進(jìn)神經(jīng)元存活并刺激內(nèi)源性神經(jīng)發(fā)生。
- 抗炎與免疫調(diào)節(jié):MSCs能將中樞神經(jīng)系統(tǒng)內(nèi)的小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞從促炎表型(M1/A1)轉(zhuǎn)化為神經(jīng)保護(hù)表型(M2/A2),從而減輕慢性神經(jīng)炎癥。
- 促進(jìn)Aβ清除:MSCs可增強(qiáng)小膠質(zhì)細(xì)胞對(duì)Aβ斑塊的吞噬作用,并分泌或誘導(dǎo)腦啡肽酶等降解酶,幫助減少腦內(nèi)Aβ負(fù)荷。
- 抗凋亡與抗氧化:通過(guò)旁分泌信號(hào)調(diào)節(jié)細(xì)胞存活通路,抑制神經(jīng)元凋亡,并分泌抗氧化物質(zhì)以減輕氧化應(yīng)激損傷。
- 促進(jìn)血管新生與修復(fù):分泌VEGF、FGF-2等血管生成因子,有助于改善腦血流灌注和血管功能,針對(duì)AD中常見的血管功能障礙。
研究目的與方法
盡管臨床前研究顯示了MSCs治療AD的潛力,但由于臨床試驗(yàn)數(shù)量有限且多處于早期階段,其在患者中的實(shí)際獲益仍不明確。本綜述旨在從循證醫(yī)學(xué)角度,系統(tǒng)評(píng)估MSCs治療AD的當(dāng)前臨床療效并展望其前景。
我們系統(tǒng)檢索了2011年1月至2025年6月期間,收錄于ClinicalTrials.gov、PubMed、Web of Science和SCOPUS數(shù)據(jù)庫(kù)的文獻(xiàn)與注冊(cè)試驗(yàn),關(guān)鍵詞包括“阿爾茨海默病”、“間充質(zhì)干細(xì)胞”和“臨床試驗(yàn)”。經(jīng)篩選,最終納入17項(xiàng)臨床試驗(yàn)及4篇相關(guān)論文進(jìn)行深度分析(圖1)。
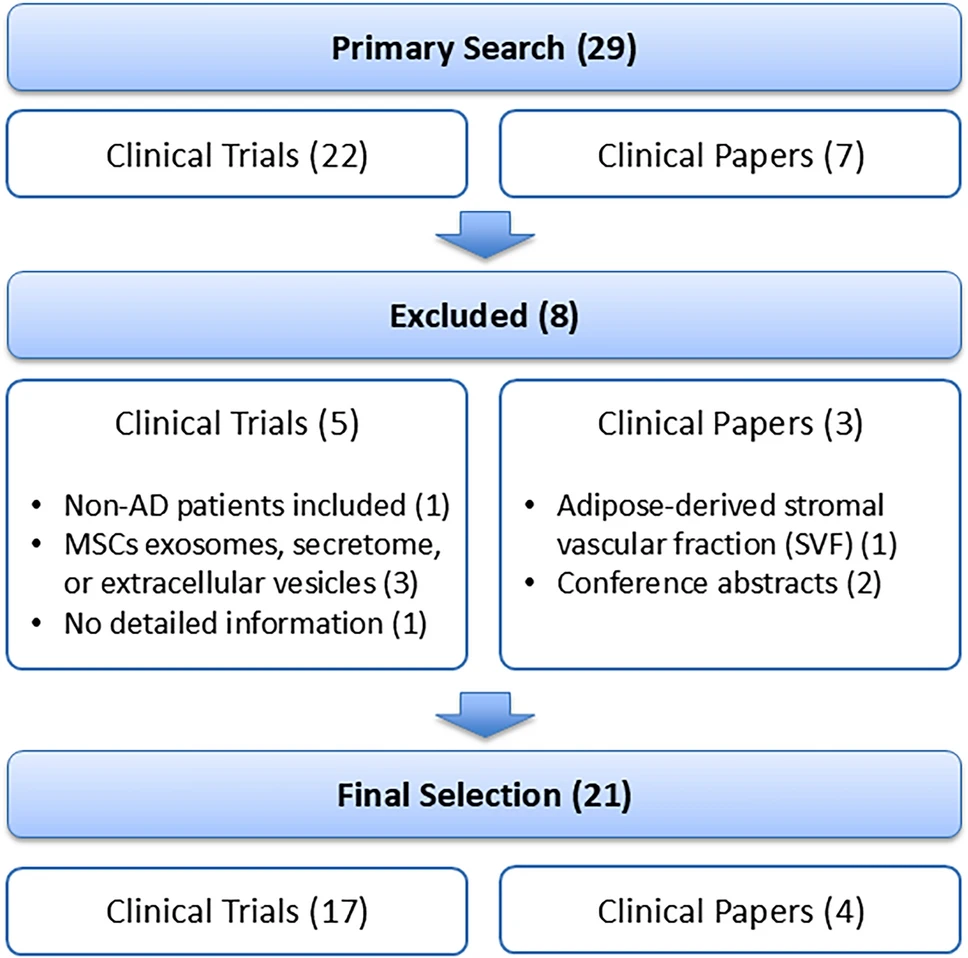
基于現(xiàn)有數(shù)據(jù)的間充質(zhì)干細(xì)胞治療阿爾茨海默病的臨床試驗(yàn)深度分析
試驗(yàn)時(shí)間線與地理分布明細(xì):在明確提及年份的17項(xiàng)試驗(yàn)中,研究活動(dòng)呈持續(xù)但低量的分布。具體而言,2011年有1項(xiàng),2025年計(jì)劃有2項(xiàng),其余年份(介于其間)每年約有0至3項(xiàng)試驗(yàn)啟動(dòng)或進(jìn)行,表明這是一個(gè)長(zhǎng)期但未形成爆發(fā)式增長(zhǎng)的研究領(lǐng)域。從地理分布看,美國(guó)主導(dǎo)了超過(guò)一半(9項(xiàng),52.9%) 的研究,韓國(guó)貢獻(xiàn)了超過(guò)三分之一(6項(xiàng),35.3%),中國(guó)進(jìn)行了2項(xiàng)(11.8%)。與此相關(guān)的4篇臨床論文發(fā)表于2015年(2篇)、2021年和2023年,印證了該領(lǐng)域超過(guò)十年的持續(xù)關(guān)注度(圖2)。
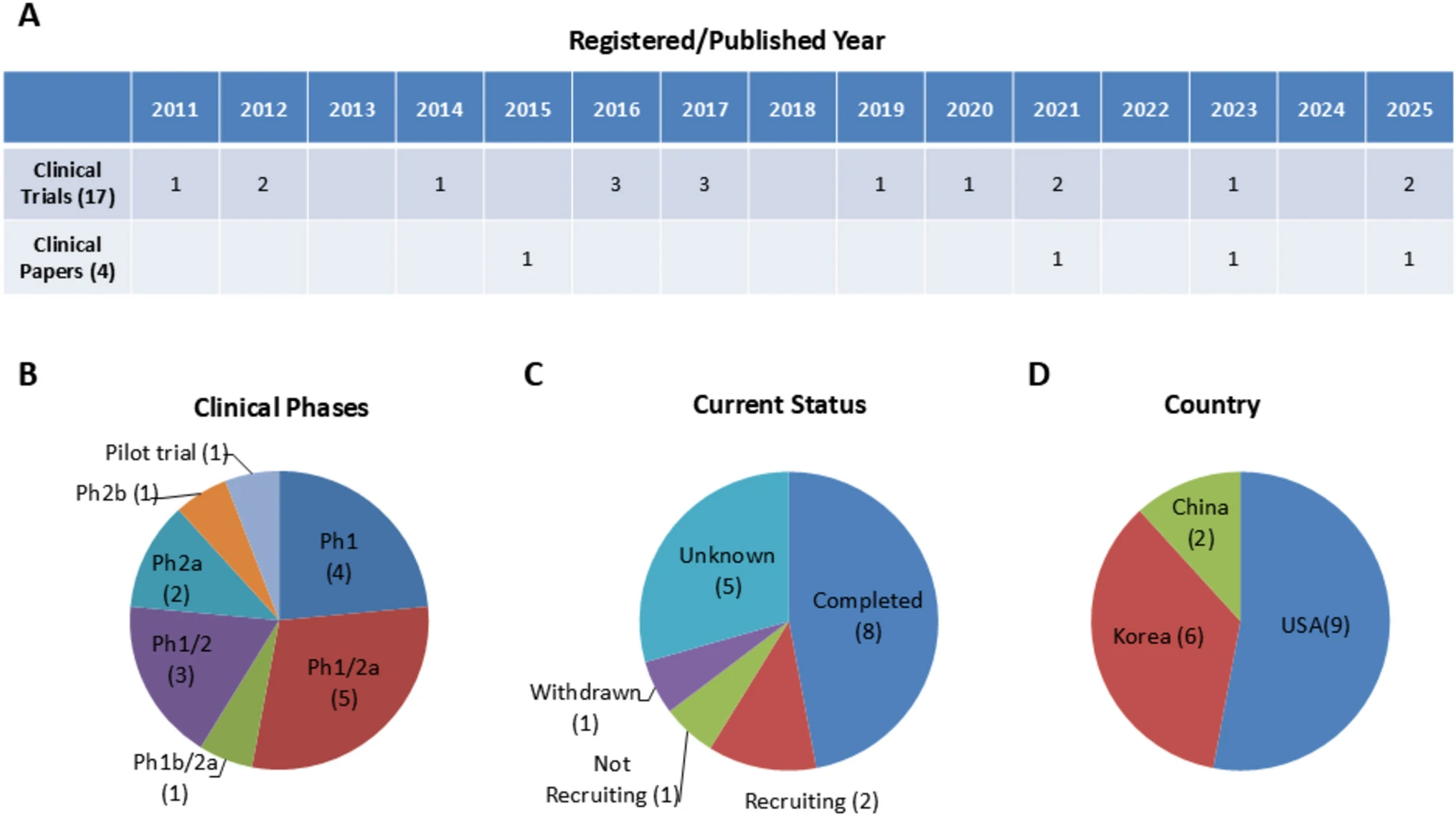
研發(fā)階段、狀態(tài)與細(xì)胞來(lái)源具體構(gòu)成:所有試驗(yàn)均處于早期研發(fā)階段,其具體構(gòu)成如下:I期4項(xiàng)(23.5%),I/IIa期5項(xiàng)(29.4%),I/II期3項(xiàng)(17.6%),IIa期2項(xiàng)(11.8%),Ib/IIa期、IIb期及“試點(diǎn)”階段各1項(xiàng)(各占5.9%),確無(wú)III期試驗(yàn)(表1)。

關(guān)于試驗(yàn)狀態(tài),已完成的項(xiàng)目最多,共8項(xiàng)(47.1%);進(jìn)行中3項(xiàng)(17.6%,其中2項(xiàng)招募中,1項(xiàng)已停止招募);1項(xiàng)因新冠疫情終止(5.9%);剩余5項(xiàng)狀態(tài)未知(29.4%)。
所使用的MSC來(lái)源多樣,具體為:異體臍帶血(UCB)來(lái)源最多,共5項(xiàng)(29.4%),自體脂肪組織來(lái)源4項(xiàng)(23.5%),異體骨髓(BM)來(lái)源3項(xiàng)(17.6%),異體胎盤來(lái)源1項(xiàng)(5.9%),另有1項(xiàng)來(lái)源不明。
給藥途徑、劑量與受試方案的詳細(xì)差異:給藥途徑與細(xì)胞來(lái)源高度關(guān)聯(lián):所有5項(xiàng)使用臍帶血MSC的試驗(yàn)均采用直接腦部注射(其中2項(xiàng)為立體定向注射,3項(xiàng)為經(jīng)Ommaya儲(chǔ)液囊腦室內(nèi)注射)。其余12項(xiàng)使用其他來(lái)源MSC的試驗(yàn)則全部采用靜脈注射。
在治療方案上,單次注射細(xì)胞劑量范圍很寬,為3×10^6至2×10^8個(gè)細(xì)胞。大多數(shù)試驗(yàn)采用多次注射方案(最多達(dá)9次),僅4項(xiàng)試驗(yàn)為單次注射。隨訪時(shí)間最短為10周,多數(shù)集中在12至52周之間,其中一項(xiàng)隨訪時(shí)間最長(zhǎng),為65周。受試者年齡范圍主要集中在50至85歲。
間充質(zhì)干細(xì)胞治療17項(xiàng)阿爾茨海默病的臨床試驗(yàn)總結(jié)
以下內(nèi)容逐一總結(jié)了17項(xiàng)臨床試驗(yàn)的詳細(xì)信息 。每項(xiàng)試驗(yàn)的條目包括NCT編號(hào)、細(xì)胞類型、試驗(yàn)階段/設(shè)計(jì)、年份和當(dāng)前狀態(tài)、受試者人數(shù)、劑量、給藥方案、隨訪期以及結(jié)果(如有)。下文還根據(jù)所用細(xì)胞類型總結(jié)了每項(xiàng)臨床試驗(yàn)的關(guān)鍵信息。
同種異體臍帶血間充質(zhì)干細(xì)胞(hUCB-MSCs)的5項(xiàng)試驗(yàn)
這組試驗(yàn)主要由韓國(guó)的“NEUROSTEM-AD”系列研究構(gòu)成,采用腦部局部給藥。
NCT01297218 (1期):開放標(biāo)簽,單中心。2015年完成,9名患者。分為低(3×10?細(xì)胞)高(6×10?細(xì)胞)劑量組,經(jīng)立體定向注射至海馬和楔前葉。24個(gè)月隨訪顯示安全,并觀察到潛在療效信號(hào)。
NCT01696591 (觀察性隨訪):作為上一試驗(yàn)的長(zhǎng)期隨訪,2015年完成,隨訪至24個(gè)月,并納入3名未治療者作為對(duì)照。
NCT02054208 (1/2a期):雙盲,單中心。2021年完成。分兩階段:開放標(biāo)簽1期(低1×10?、高3×10?細(xì)胞/次)和隨機(jī)2a期(高劑量組 vs 安慰劑組)。通過(guò)Ommaya囊腦室內(nèi)(ICV) 注射,共3次。結(jié)果顯示安全,高劑量組部分認(rèn)知評(píng)分有改善趨勢(shì)。
NCT03172117 (長(zhǎng)期隨訪):上一試驗(yàn)的延伸隨訪,2021年完成,計(jì)劃進(jìn)行36個(gè)月電話隨訪。
NCT04954534 (探索性療效研究):單臂研究,計(jì)劃讓之前試驗(yàn)的安慰劑組交叉接受高劑量(3×10?細(xì)胞/次,ICV注射3次)治療。狀態(tài)與結(jié)果未知。
自體脂肪間充質(zhì)干細(xì)胞(AdMSCs)的4項(xiàng)試驗(yàn)
這組試驗(yàn)主要采用靜脈注射,以“AstroStem”為代表,探索多次給藥的方案。
NCT03117738 (I/II期):隨機(jī)雙盲,安慰劑對(duì)照。已完成(結(jié)果發(fā)布于網(wǎng)站)。31名患者(21治療,10安慰劑),每次靜脈注射2×10?個(gè)細(xì)胞,共9次,隨訪52周。
NCT04482413 (2b期):隨機(jī)雙盲,安慰劑對(duì)照。狀態(tài)未知。計(jì)劃招募約100人,方案類似(靜脈注射9次),計(jì)劃隨訪至40周。
NCT04228666 (1/2a期):開放標(biāo)簽。因新冠疫情在招募前已撤回。原計(jì)劃招募24人,靜脈注射4次(2×10?細(xì)胞/次)。
NCT06775964 (1b/2a期):開放標(biāo)簽,單組。正在招募,預(yù)計(jì)2026年完成。計(jì)劃招募12名前驅(qū)期患者,靜脈注射4次(2×10?細(xì)胞/次),隨訪48周。
同種異體臍帶間充質(zhì)干細(xì)胞(UC MSCs)的3項(xiàng)試驗(yàn)
這三項(xiàng)試驗(yàn)均采用靜脈注射,但方案設(shè)計(jì)差異較大。
NCT01547689 (I/II期):開放標(biāo)簽,自身對(duì)照。已完成但結(jié)果未發(fā)表。30名中重度患者,接受8次靜脈輸注(2×10?細(xì)胞/次,療程復(fù)雜),隨訪僅10周。
NCT02672306 (I/II期):隨機(jī)雙盲,安慰劑對(duì)照。狀態(tài)與結(jié)果未知。計(jì)劃招募16名輕中度患者,靜脈注射8次(2×10?細(xì)胞/次),隨訪48周。
NCT04040348 (I期):前瞻性開放標(biāo)簽。已完成治療(2021年),結(jié)果未發(fā)表。6名輕度患者,接受4次靜脈輸注(間隔13周),隨訪期未明確。
同種異體胎盤間充質(zhì)干細(xì)胞的1項(xiàng)試驗(yàn)
NCT02899091 (1/2a期):隨機(jī)雙盲,安慰劑對(duì)照。狀態(tài)為“進(jìn)行中,不再招募”。計(jì)劃招募24名輕中度患者,進(jìn)行單次或兩次靜脈輸注(具體劑量未明確),隨訪48周。結(jié)果未公布。
同種異體骨髓間充質(zhì)干細(xì)胞的3項(xiàng)試驗(yàn)
這組以“Lomecel-B”為代表,采用靜脈注射,研究設(shè)計(jì)較為精細(xì)。
NCT02600130 (I期):隨機(jī)雙盲,安慰劑對(duì)照。2023年發(fā)表結(jié)果。33名患者,分單次低劑量(2×10?)、高劑量(1×10?)及安慰劑組,隨訪52周。證實(shí)安全,并顯示部分生物標(biāo)志物改善。
NCT05233774 (2a期):雙盲,安慰劑對(duì)照。2025年發(fā)表結(jié)果。48名患者,分4組,比較了單次 vs. 4次(低劑量2.5×10?細(xì)胞/次或高劑量1×10?細(xì)胞/次)靜脈輸注方案。
NCT02833792 (IIa期):隨機(jī)單盲,安慰劑對(duì)照交叉設(shè)計(jì)。狀態(tài)不明。計(jì)劃招募40人,單次靜脈輸注(按體重1.5×10?細(xì)胞/kg),交叉期6個(gè)月,總隨訪18個(gè)月。
細(xì)胞類型未知的1項(xiàng)試驗(yàn)
NCT06781333 (試點(diǎn)研究):開放標(biāo)簽,單組。截至2025年5月仍在招募。8名伴有嚴(yán)重行為癥狀的AD患者,接受單次靜脈輸注(來(lái)源與劑量均未明確),作為輔助治療,隨訪12周。結(jié)果未公布。
從選定部分的臨床試驗(yàn)驗(yàn)證其安全性和有效性
在納入綜述的17項(xiàng)臨床試驗(yàn)中,共有7項(xiàng)試驗(yàn)的結(jié)果發(fā)表在4篇臨床論文中,另有1項(xiàng)試驗(yàn)的結(jié)果發(fā)布于ClinicalTrials.gov網(wǎng)站(匯總于表3)。為提供關(guān)鍵證據(jù)概覽,下文將首先概要介紹這5項(xiàng)已發(fā)表數(shù)據(jù)的主要結(jié)果,其詳細(xì)分析與討論將在明天的文章中展開。
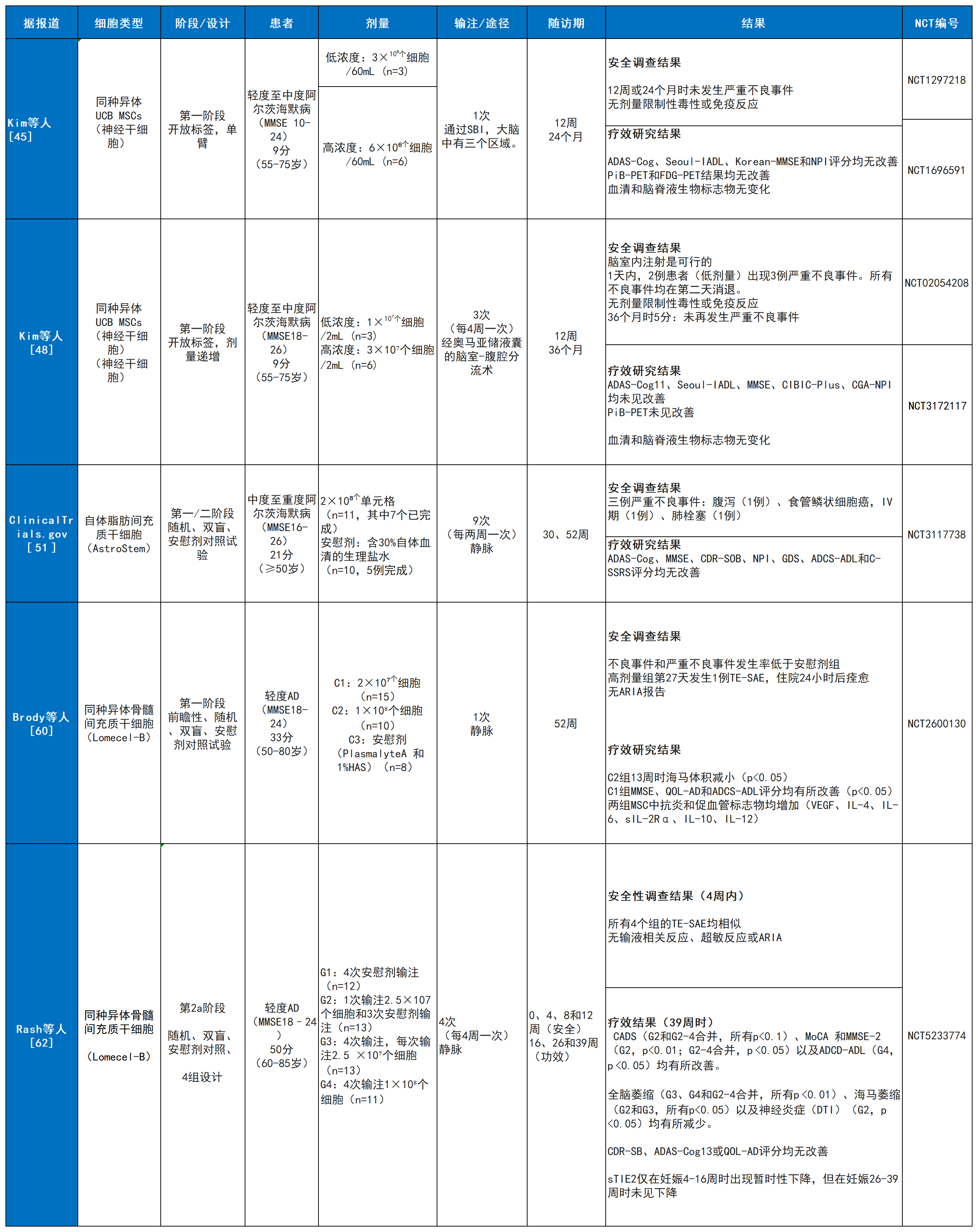
安全性總結(jié)(涵蓋所有已公布結(jié)果的7項(xiàng)試驗(yàn))
綜合所有已公布數(shù)據(jù)的試驗(yàn),間充質(zhì)干細(xì)胞療法在阿爾茨海默病患者中表現(xiàn)出良好的安全性。具體而言:
- 采用臍帶血MSCs(產(chǎn)品NEUROSTEM-AD) 的4項(xiàng)試驗(yàn)(采用立體定向海馬注射的NCT01297218與NCT01696591,以及采用腦室內(nèi)注射的NCT02054208與NCT03172117)均報(bào)告治療安全,僅出現(xiàn)暫時(shí)性嚴(yán)重不良事件。
- 采用骨髓MSCs(產(chǎn)品Lomecel-B)的2項(xiàng)試驗(yàn)(NCT02600130與NCT05233774)同樣證實(shí)其安全性。
- 采用脂肪MSCs(產(chǎn)品AstroStem) 的試驗(yàn)(NCT03117738)結(jié)果也顯示安全性良好。
有效性總結(jié)(結(jié)果存在差異)
在有效性方面,不同細(xì)胞來(lái)源的產(chǎn)品結(jié)果不一致:
- 骨髓MSCs(Lomecel-B)顯示積極信號(hào):試驗(yàn)NCT02600130和NCT05233774報(bào)告了在AD病理生理或認(rèn)知功能方面的顯著改善。
- 臍帶血與脂肪MSCs未顯示顯著療效:采用NEUROSTEM-AD的4項(xiàng)試驗(yàn)(NCT01297218NCT01696591,NCT02054208, NCT03172117)及采用AstroStem的試驗(yàn)(NCT03117738)均未觀察到明顯的治療效果。
這種差異表明,療效可能與特定的細(xì)胞類型、產(chǎn)品制備工藝或給藥途徑密切相關(guān)。
核心問(wèn)答與未來(lái)展望
當(dāng)前核心結(jié)論:安全初證,療效待明
綜上所述,間充質(zhì)干細(xì)胞療法治療阿爾茨海默病已從實(shí)驗(yàn)室步入臨床探索階段,其短期安全性已獲初步支撐,為后續(xù)研究奠定了基礎(chǔ)。然而,關(guān)于其療效的決定性證據(jù)仍然缺乏。MSCs的核心價(jià)值在于其多靶點(diǎn)作用機(jī)制,為應(yīng)對(duì)AD的復(fù)雜性提供了新思路。當(dāng)前領(lǐng)域的首要任務(wù)是跨越“證據(jù)鴻溝”。
未來(lái)5-10年,通過(guò)推進(jìn)大規(guī)模確證性臨床試驗(yàn),并同步探索外泌體等創(chuàng)新策略,將最終明確MSCs在AD治療格局中的定位。無(wú)論結(jié)果如何,這一探索過(guò)程所積累的深刻見解,都將對(duì)神經(jīng)退行性疾病治療領(lǐng)域產(chǎn)生重要影響。
參考資料:
[1]:Kim, AL., Lee, W.K., Kwon, S. et al. Therapeutic Efficacy of Mesenchymal Stem Cells (MSCs) on Alzheimer’s Disease: Review of Clinical Results. Tissue Eng Regen Med (2026). https://doi.org/10.1007/s13770-025-00782-1
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信