
在2025年3月22日舉辦的第二屆博鰲樂城干細胞大會上,海南博鰲樂城國際醫療旅游先行區首次公布了膝骨關節炎干細胞治療的官方定價為3.6萬元/次,這一舉措標志著中國干細胞治療領域邁入規范化與透明化的新階段。
價格的明確不僅緩解了患者對高昂費用的擔憂,更推動了行業從“無序高價”向“可及性醫療”轉型。然而,價格透明僅是醫療技術普惠的第一步,療效的標準化評估體系建立同樣關鍵。
近期發布的《人臍帶間充質干細胞治療膝骨性關節炎臨床應用指南》(T/ZGCIT015-2024)首次系統性地提出了治療適應癥、禁忌癥、注射方案及療效追蹤等核心標準,為臨床實踐提供了科學依據,確保治療的安全性與有效性。
本文將從價格政策與療效評估雙重視角,探討這一里程碑事件對患者、行業及未來醫療發展的深遠影響。
海南博鰲樂城干細胞治療膝骨骨關節炎價格透明化的意義,患者信任和行業秩序的重塑作用
在海南博鰲干細胞治療膝骨關節炎的官方定價公布前,市場價格存在較大差異且缺乏統一標準。
根據公開信息,國內部分醫療機構的干細胞治療價格波動較大,例如瓊海某醫院在2022年推出的PRP(富血小板血漿)治療退行性關節炎價格為8000元(原價13750元),而干細胞治療價格則普遍在3萬至10萬元之間。例如,瓊海醫院2025年3月的干細胞注射價格表顯示,關節炎治療費用約為5萬至10萬元,而新疆圖木舒克醫院的同類項目報價在3萬至5萬元。
國際市場上,韓國、美國等地的干細胞療法價格更高,如韓國的Cartistem約8萬至10萬元,美國的MacI則達20萬至30萬元。這種價格混亂主要源于技術標準不統一、缺乏監管以及患者對療效的信息不對稱,導致部分機構存在高價牟利或夸大宣傳的現象。
2025年3月,海南博鰲樂城國際醫療旅游先行區首次公布官方定價,將臍帶間充質干細胞治療膝骨關節炎的價格定為3.6萬元/次。這一舉措具有里程碑意義:
- 重建患者信任:透明化定價消除了市場上的模糊空間,使患者能夠清晰了解治療成本,減少對 “天價治療” 的疑慮,增強對正規醫療機構的信任。
- 規范行業秩序:官方定價為行業提供了明確的參考標準,遏制了部分機構隨意定價的亂象,推動干細胞治療從 “灰色地帶” 轉向規范化發展。
- 促進技術普及:合理的定價降低了治療門檻,尤其對比國際高價,3.6萬元的價格更具可及性,有望加速干細胞療法的臨床應用和推廣。
- 推動創新與監管:定價的透明化也倒逼行業提升技術標準和服務質量,促使更多企業通過合規研發和臨床試驗爭取政策支持,形成良性競爭環境。
綜上,官方定價不僅是市場秩序的 “錨點”,更是推動干細胞產業從無序探索邁向成熟發展的關鍵一步,為患者和行業帶來雙重利好。
花3.6萬/次運用干細胞治療膝骨骨關節炎,效果如何?從標準化評估其療效的要求有哪些?
干細胞治療膝骨骨關節炎,效果如何?
2024年7月25日,山東省紅十字會介入醫院在國際期刊《Stem Cells and Regenerative Medicine》上發布了一篇《臍帶間充質干細胞局部注射治療膝關節損傷的療效及潛在機制》的研究結果。

研究結果表示:采用臍帶間充質干細胞進行關節腔內注射治療,治療后患者關節功能得到有效改善,疼痛程度減輕,且無明顯不良反應,且臍帶間充質干細胞治療組療效明顯高于常規治療組。研究組治療后1個月、2個月FMA評分顯示療效優于對照組。研究組有效率高于對照組。疼痛評分研究組治療后炎癥反應程度明顯低于參照組,差異有統計學意義。
從標準化評估干細胞治療膝骨骨關節炎療效的要求有哪些?
近日,《世界骨科雜志》發表了一篇關于“間充質干細胞治療及其對骨關節炎療效的標準化評估要求”的文章[1]。

該文章強調了間充質干細胞可以緩解骨關節炎癥狀,甚至再生軟骨,從而有可能逆轉疾病。MSC注射是一種新穎且侵入性較小的替代方法,可替代軟骨細胞移植或關節成形術等傳統治療方法,具有成本低、風險低、結果良好等特點,為OA患者提供了一種有前途的方法。
此外,還強調了在進行干細胞治療膝骨關節炎之前必須仔細考慮療效評估標準、異質性、安全性和其他因素,以進一步推進MSC治療OA的臨床轉化。
影響間充質干細胞治療骨關節炎療效的三大因素如下圖所示:
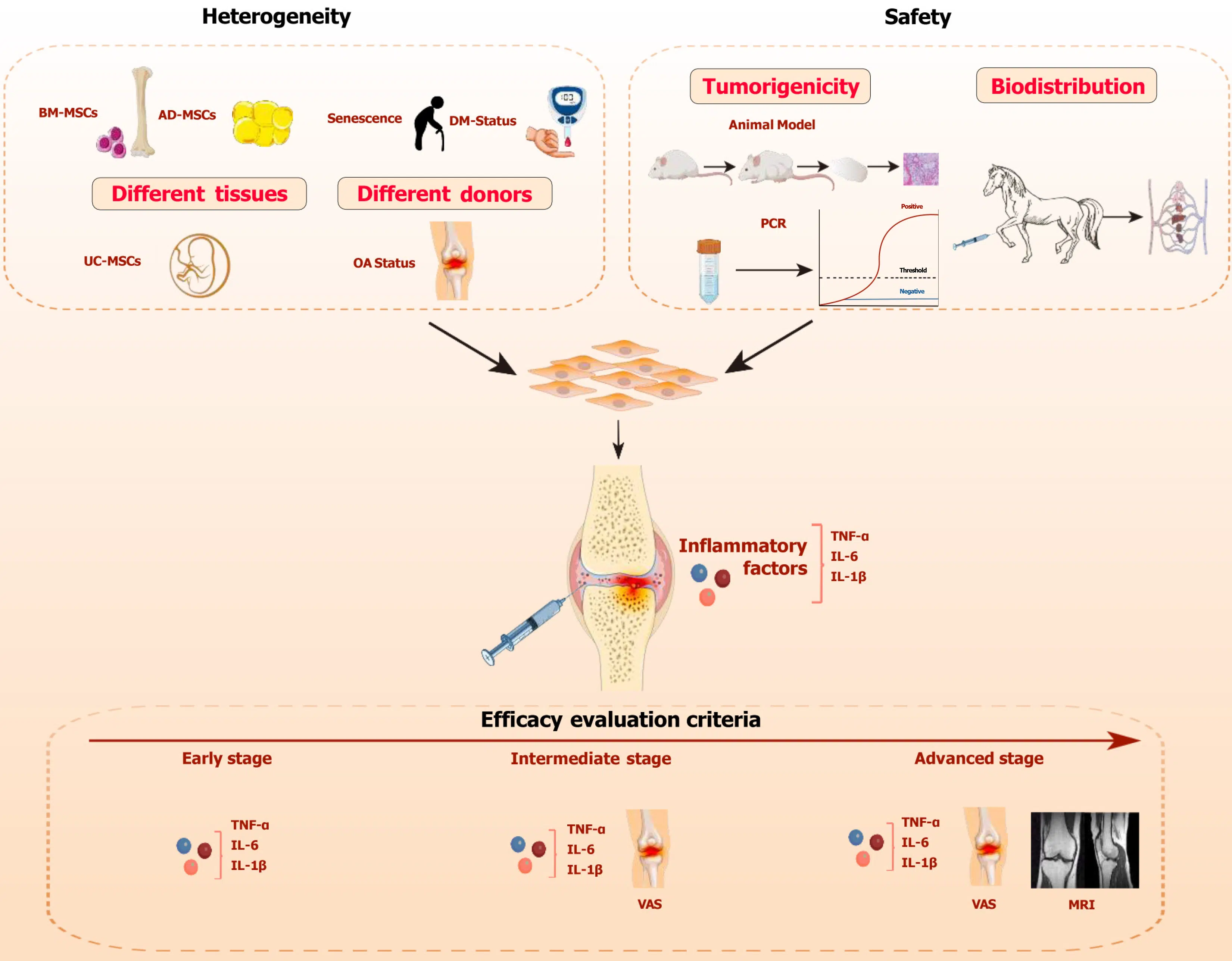
MSC:間充質干細胞;OA:骨關節炎;BM-MSC:骨髓間充質干細胞;AD-MSC:脂肪組織來源的間充質干細胞;UC-MSC:臍帶來源的間充質干細胞;IL:白細胞介素;TNF-α:腫瘤壞死因子-α;VAS:視覺模擬量表;MRI:磁共振成像。
虛線框突出顯示了需要考慮的三個關鍵因素:間充質干細胞 (MSCs) 的異質性、MSC的安全性以及評估其療效的標準。異質性包括組織異質性和供體異質性。安全性包括致瘤性和生物分布。水平紅色箭頭表示骨關節炎的進展時間線,每個階段采用不同的療效評估標準。
考慮因素一:療效評價標準
研究表明療效評估需突破傳統結構修復視角,重視炎癥與免疫調控機制;標準化評估體系應納入多維度指標(生物標志物+影像+癥狀),并針對疾病階段動態調整權重。
在主觀量表方面,常用于評估OA嚴重程度的主觀量表(如VAS疼痛評分)受患者主觀感知影響,存在較大個體差異;影像學隨訪雖能通過軟骨結構變化反映治療效果,但OA不僅是關節退行性疾病,更是一種由全身性炎癥驅動的慢性炎癥狀態,因此存在局限性。
炎癥標志物的核心價值
在OA進展中,高水平的促炎因子如腫瘤壞死因子-α(TNF-α)、白介素(IL)-1β和IL-6是導致軟骨細胞凋亡、軟骨基質降解、軟骨塌陷及滑膜浸潤的關鍵驅動因素。MSC通過分泌前列腺素E2抑制核因子κB(NF-κB)的轉錄激活,減少促炎因子釋放,同時分泌TNF-α刺激基因6蛋白、IL-1受體拮抗劑等抗炎因子緩解炎癥反應。研究表明,IL-10、IL-1β和TNF-α的mRNA表達水平下降與OA癥狀緩解相關。
MSC可能主要通過調控炎癥與免疫反應(而非依賴其軟骨分化潛能)抑制OA進展。OA患者接受MSC治療后觀察到的軟骨體積增加,可能是MSC通過抑制關節腔內炎性因子及免疫調節(如MSC調控巨噬細胞從M1向M2極化,啟動組織再生修復間接實現的。
因此,短期內(如12個月)影像學變化可能無法作為及時有效的療效指標。
分階段綜合評估體系早期(無癥狀/輕微癥狀):綜上,在OA早期臨床階段(如Kellgren-Lawrence分級0級),患者可能僅表現為輕微或無顯著癥狀的短暫性不適。對此類病例,建議通過監測TNF-α、IL-1β和IL-6等炎癥標志物的趨勢評估療效:若炎癥標志物呈下降趨勢或維持同一區間,表明治療有效延緩了OA進展甚至逆轉了關節腔炎癥;若持續升高,則提示治療無效且疾病進展。當患者出現持續性顯著疼痛時,表明疾病已進入中期,此時影像學檢查常無顯著變化。
中期(顯著疼痛):中期以臨床癥狀突出為特點,需聯合炎癥標志物與VAS評分評估:疼痛是此階段的主要癥狀,VAS應為核心指標,但由于其主觀性易受患者偏倚影響,需以炎癥標志物為次要指標;當患者無法感知疼痛顯著變化時,可通過炎癥標志物趨勢判斷療效。
晚期(影像學改變明確):評估需結合影像學檢查與炎癥標志物、VAS進行綜合判斷:影像學評估中,軟骨體積變化被視為療效金標準,但短期內無法觀測到軟骨改變,因此聯合VAS與炎癥標志物可更及時評估疾病進展與療效(圖1)。
核心結論:建立基于OA病理機制的分階段、多維度療效評估框架(炎癥標志物為主觀與影像指標提供生物學驗證),是提升干細胞治療標準化與可信度的關鍵。
考慮因素二:異質性
間充質干細胞(MSC)的異質性受供體年齡、代謝狀態及病理生理狀態等因素影響顯著,導致治療效果存在差異。
Kristjánsson等雖證實了MSC的有效性與安全性,但未探討異質性對臨床結局的影響。Soufan等強調組織來源差異,指出脂肪來源MSC(AD-MSC)療效優于臍帶(UC-MSC)與骨髓來源MSC(BM-MSC),為臨床來源選擇提供依據。
此外,選擇MSC產品時,不同供體間的異質性亦至關重要。衰老個體的MSC自身功能衰退且干性逐漸喪失;同時,關節腔內衰老細胞積聚并釋放衰老相關分泌表型(SASP),通過NF-κB依賴途徑誘導MSC早衰,進而影響其功能。
因此異質性主要受供體因素和細胞來源影響
- 供體因素:年齡(老年供體MSC功能衰退)、代謝狀態(如糖尿病高血糖抑制MSC存活與功能)、遺傳背景(特定基因過表達降低MSC效能)及病理微環境(如OA關節腔SASP誘導MSC早衰)是異質性的核心驅動因素。
- 組織來源差異:AD-MSC療效優于UC-MSC與BM-MSC,提示臨床需優先選擇特定組織來源。
結論:MSC異質性是制約其臨床療效可重復性的關鍵瓶頸。通過供體標準化篩選、基因工程改造及保存技術優化構建“低異質性MSC產品”,并建立動態監測體系,是推動干細胞治療從實驗走向標準化臨床應用的核心路徑。
考慮因素三:安全
截至目前,ClinicalTrials.gov上已注冊了14,000多項MSC相關臨床研究。歐盟已批準使用MSC治療克羅恩病相關的腸外瘺,而韓國、日本和加拿大已批準使用MSC療法治療移植物抗宿主病。Cartistem (MEDIPOST) 含有同種異體UC-MSC和透明質酸水凝膠,是全球唯一獲批用于治療肌肉骨骼疾病的MSC產品。
臨床結果表明,患者在接受Cartistem治療后,可出現透明樣軟骨形成。患者的國際軟骨修復學會評分、VAS評分、西安大略和麥克馬斯特大學骨關節炎指數 (WOMAC) 評分和國際膝關節文獻委員會評分均有顯著改善。
基于現有的多項臨床研究,不可否認關節內注射間充質干細胞已證實具有長期治療效果。

在一項前瞻性雙盲隨機對照IIb期臨床試驗中,接受關節內MSC注射的實驗組在治療六個月后WOMAC評分明顯改善,軟骨損傷明顯延遲。在另一項比較關節內MSC注射和透明質酸注射療效的研究中,治療12個月后,接受MSC注射的患者的軟骨體積明顯大于接受透明質酸治療的患者。
盡管MSC應用日益廣泛,其臨床治療安全性仍存爭議。兩篇文獻作者對安全性關注較少。根據國際干細胞研究學會《干細胞研究與臨床轉化指南》,MSC臨床試驗前需完成致瘤性與生物分布臨床前研究以確保安全有效,但目前缺乏MSC產品安全性與療效的標準化評估方法。
主要風險是其潛在致瘤性:部分臨床試驗報告短期安全性良好,但多數研究未評估長期致瘤風險。
- 一項異體人臍帶MSC超高劑量給藥26周的臨床前致瘤性評估中,未觀察到腫瘤形成證據;
- 另一項隨訪96周的脂肪MSC治療OA研究亦未檢測到腫瘤。
結論:MSC治療安全性需平衡短期療效與長期風險,通過致瘤性快速檢測、生物分布精準追蹤及免疫反應動態監控構建“預防-評估-干預”一體化安全體系,是實現其臨床轉化可持續發展的關鍵。
價格透明化與療效標準化雙軌并行:博鰲樂城干細胞治療膝骨關節炎的破局之道
博鰲樂城干細胞治療膝骨關節炎的官方定價公布,不僅是醫療費用透明化的里程碑,更標志著中國在干細胞治療規范化進程中邁出關鍵一步。價格的可及性為患者提供了新希望,但療效的標準化評估體系才是確保這一希望轉化為真實臨床獲益的核心保障。
從炎癥標志物的動態監測、影像學與主觀量表的聯合應用,到異質性控制與長期安全追蹤,標準化評估要求的落地需要多方協同:政策端需強化監管框架,推動全國性療效評估指南的制定;技術端應加速創新,整合多組學分析與智能監測工具;臨床端則需建立真實世界數據平臺,實現療效與風險的動態反饋。
作為醫療特區,博鰲樂城在價格與療效“雙透明”的探索中,正為行業樹立標桿。未來,隨著評估標準的細化與技術的迭代,干細胞治療有望從“個體化嘗試”走向“標準化普惠”,讓更多膝骨關節炎患者真正受益于再生醫學的突破。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。
參考資料:[1]:Wang YC, Cheng JB, Feng ML. Requirements for standardizing the assessment of mesenchymal stem cell therapy and its effects on osteoarthritis. World J Orthop. 2025 Mar 18;16(3):104451. doi: 10.5312/wjo.v16.i3.104451. PMCID: PMC11924026.



 掃碼添加官方微信
掃碼添加官方微信