糖尿病與干細胞治療前景:糖尿病 (DM) 是一種慢性代謝性疾病,其特征是由于胰島素生成或作用缺陷導(dǎo)致的持續(xù)性高血糖。
其主要類型為1型糖尿病 (T1DM,自身免疫性β細胞破壞) 和2型糖尿病 (T2DM,胰島素抵抗伴β細胞功能障礙),影響著全球數(shù)百萬患者,并導(dǎo)致嚴重并發(fā)癥。當(dāng)前的胰島素替代療法和對癥管理無法解決潛在的細胞功能障礙,這推動了對再生醫(yī)學(xué)策略的探索,干細胞療法因此成為研究熱點。

最有希望的干細胞候選者包括具有免疫調(diào)節(jié)和再生潛力的間充質(zhì)干細胞 (MSC),以及能分化為功能性β細胞的多能干細胞 (PSC)。
近年來,細胞重編程、分化方案和封裝技術(shù)的進步顯著改善了臨床前效果。盡管存在免疫排斥、細胞存活和安全性的挑戰(zhàn),但正在進行的人體試驗,特別是針對MSC的研究,展現(xiàn)出將糖尿病管理從控制癥狀轉(zhuǎn)向潛在治愈的希望。基因編輯和組織工程等新興技術(shù)有望進一步提升療效。
干細胞治療糖尿病有效嗎?17項薈萃分析超8000+患者數(shù)據(jù)證實顯著降低血糖、減少胰島素依賴
2025年7月,國際著名期刊雜志《Tissue and Cell》發(fā)表了一篇“間充質(zhì)干細胞治療糖尿病:綜述”的文章綜述[1]。

綜述研究結(jié)果表明:該綜述納入了17篇系統(tǒng)綜述和薈萃分析,涵蓋超過8,000名患者。MSC療法顯著改善了血糖控制,尤其是在2型糖尿病(T2DM)中,糖化血紅蛋白(HbA1c)降低(最高可達1.45%),胰島素需求量降低(最高可達2.05單位/千克/天)。
在1型糖尿病(T1DM)中,間充質(zhì)干細胞療法改善了C肽水平和糖化血紅蛋白(HbA1c),但對胰島素依賴性的影響各不相同。華通氏膠衍生的MSC和骨髓衍生細胞表現(xiàn)出優(yōu)異的療效,而臍帶血衍生的MSC療效較差。不良事件通常較輕(例如發(fā)燒、注射部位反應(yīng)),嚴重事件罕見,且與聯(lián)合療法有關(guān)。
研究目的與方法
本綜述系統(tǒng)整合間充質(zhì)干細胞(MSC)療法治療糖尿病的有效性及安全性證據(jù),重點剖析其臨床療效、作用機制及突破傳統(tǒng)治療局限的潛力。本綜述整合了截至2025年7月30日的相關(guān)系統(tǒng)綜述與薈萃分析(傘狀綜述)。研究依據(jù)PRISMA指南檢索PubMed/MEDLINE、Scopus及Web of Science數(shù)據(jù)庫。
納入標(biāo)準(zhǔn)限定為評估MSC療法治療T1DM/T2DM的系統(tǒng)綜述與薈萃分析,核心結(jié)局指標(biāo)包括血糖控制(HbA1c)、β細胞功能(C肽)及安全性。采用AMSTAR-2工具評價納入研究的方法學(xué)質(zhì)量,并通過三重框架(研究重疊性、臨床結(jié)局、安全性)整合證據(jù)。
文獻篩選與納入研究特征
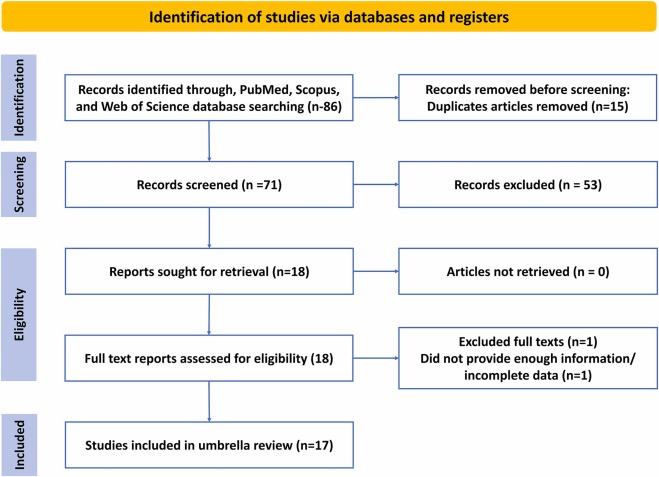
初篩獲得86項記錄,去重后保留71項進行標(biāo)題/摘要篩選,18項進入全文評估。最終17項系統(tǒng)綜述/薈萃分析符合標(biāo)準(zhǔn)(篩選流程圖見圖1),形成了本綜述的核心證據(jù)基礎(chǔ),覆蓋超過8,000名糖尿病患者。
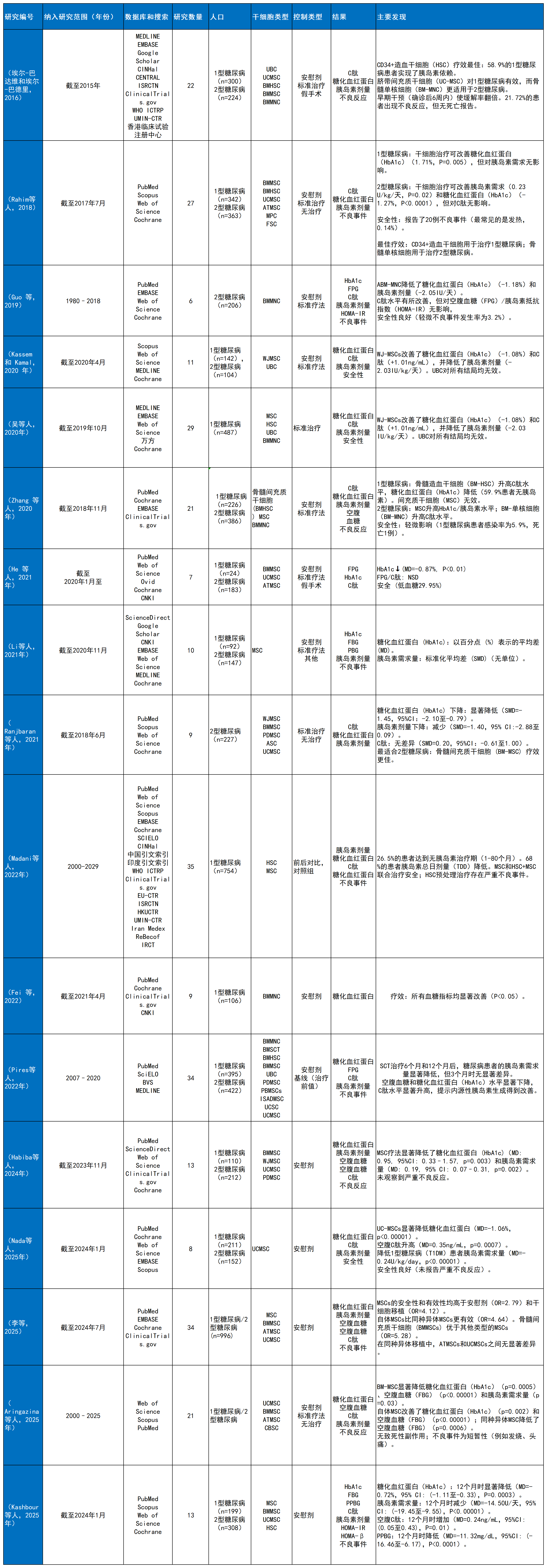
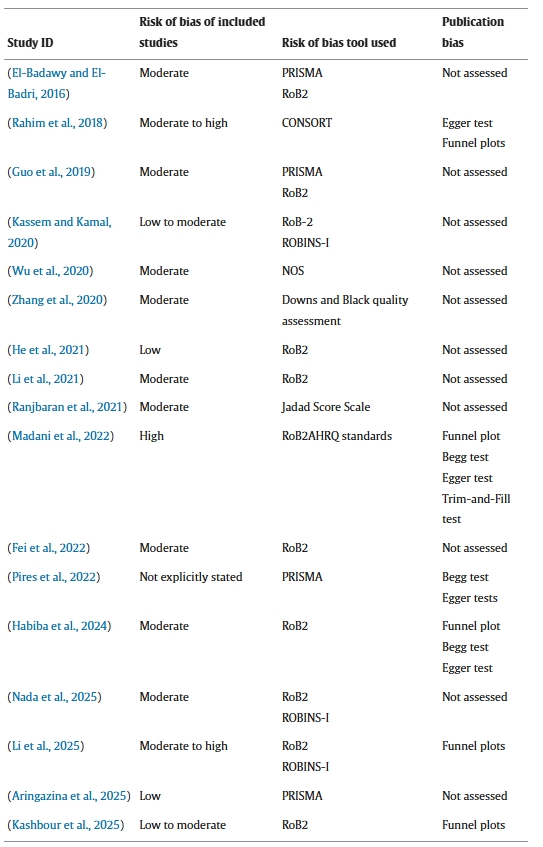
每項納入的綜述分析了6至35項原始研究,評估的干細胞類型包括:間充質(zhì)干細胞(MSC)、臍帶間充質(zhì)干細胞(UC-MSC)、骨髓來源干細胞(BM-MNCs/MSC)、脂肪干細胞(ASC)和造血干細胞(HSC)。對照組主要為安慰劑、常規(guī)治療或其它靶向治療(詳見表1研究特征總結(jié),表2偏倚評估)。
表1和表2全面概述了綜述的特征,包括人群、干預(yù)措施、對照、結(jié)果和偏倚。
方法學(xué)質(zhì)量評價結(jié)果
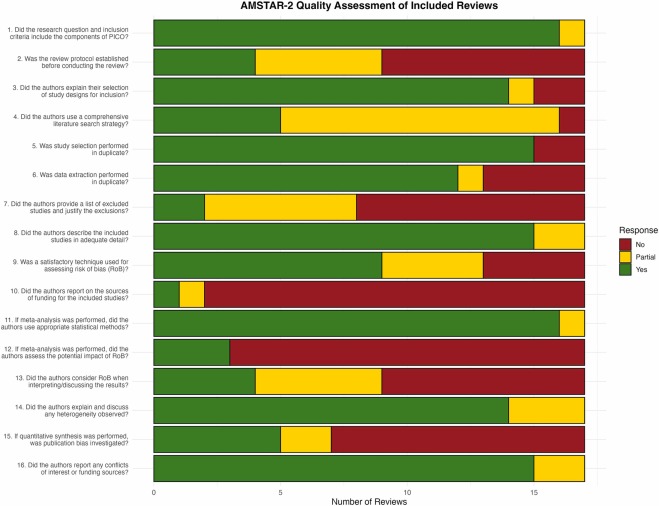
AMSTAR-2評估表明,所有綜述均在其研究問題中恰當(dāng)?shù)丶{入了PICO要素。大多數(shù)研究采用了重復(fù)研究篩選流程,并使用適當(dāng)?shù)慕y(tǒng)計方法進行了定量綜合。然而,盡管所有進行薈萃分析的綜述都充分解決了異質(zhì)性問題,但部分綜述盡管進行了定量綜合,卻未能調(diào)查出版偏倚。
圖2顯示了所有評估項目的AMSTAR-2合規(guī)率,每篇綜述的完整評分詳情見補充文件表S2。
納入系統(tǒng)評價與薈萃分析的重疊分析
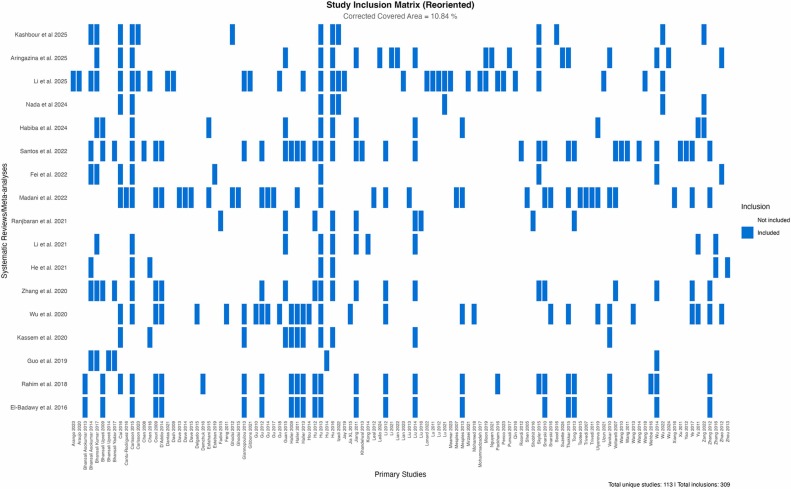
研究篩選與重疊量化:本分析納入17項薈萃分析涉及的309項原始研究引文,經(jīng)去重后獲得113項獨特研究。量化評估顯示,不同綜述間的原始研究重疊率為10.84%(校正覆蓋區(qū)域,CCA),顯著低于預(yù)設(shè)的15%冗余閾值。基于三項高影響力研究(Carlsson et al., 2015; Hu et al., 2013, 2016)的先驅(qū)性價值(首次證實干細胞糖尿病療效)、方法學(xué)嚴謹性(隨機設(shè)計/長期隨訪)及排除后對獨立性影響微弱(CCA僅降至8.01%),予以保留(詳見圖S1)。
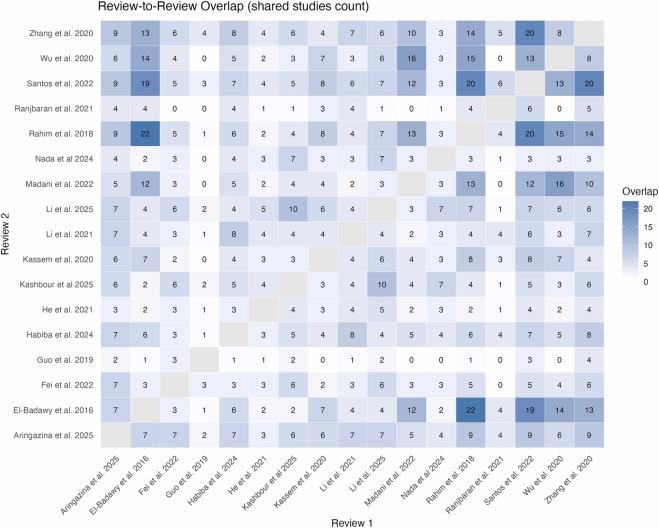
策略性取舍與證據(jù)完整性:針對最顯著的重疊案例(El-Badawy et al., 2016與Rahim et al., 2018共享22項研究),我們優(yōu)先保留后者——因其額外包含5項獨特研究。該決策通過排除重復(fù)度高但新增證據(jù)少的綜述(El-Badawy),在保證證據(jù)庫完整性的同時(圖3),有效控制了方法學(xué)冗余(圖4),實現(xiàn)了全面性與嚴謹性的最優(yōu)平衡。
干細胞治療糖尿病的臨床結(jié)果
臨床結(jié)果總結(jié)于表3中。
干細胞治療1型糖尿病的臨床療效:在T1DM患者中,間充質(zhì)干細胞療法持續(xù)改善血糖控制指標(biāo),C肽水平顯著改善,HbA1c降低1.71%(p=0.005),盡管每日胰島素需求量保持不變。使用MSC和造血干細胞 (HSC) 的聯(lián)合療法提供了更好的結(jié)果,高達26.5%的患者實現(xiàn)了胰島素依賴。
| 項目 | 主要成果 |
|---|---|
| 2型糖尿病 | HbA1c 下降最多1.45% 胰島素劑量↓2.05U/kg/天 |
| 1型糖尿病 | C肽↑ HbA1c↓1.71% 對胰島素需求的影響各不相同 |
| 性能最佳的MSC來源 | 華通氏膠間充質(zhì)干細胞 (WJ-MSCs) 骨髓單核細胞 (BM-MNCs) |
| 最不有效的MSC來源 | 臍帶血來源的 MSCs (UCB-MSCs) |
干細胞治療2型糖尿病的臨床療效:在2型糖尿病 (T2DM) 患者中,MSC療法始終表現(xiàn)出強大的療效,可將糖化血紅蛋白 (HbA1c) 降低高達1.45%,并顯著降低胰島素需求量(高達2.05U/kg/天)。沃頓膠衍生的MSC尤其有效,可顯著降低糖化血紅蛋白 (HbA1c) 并提高C肽水平。
MSC來源至關(guān)重要:沃頓膠MSC (WJ-MSCs) 和骨髓單核細胞 (BM-MNCs)在多項研究中均表現(xiàn)出最優(yōu)療效。相反,臍帶血來源的MSC (UCB-MSCs) 效果較差,甚至可能增加胰島素需求(表3總結(jié)了主要臨床結(jié)果和MSC來源比較)。
討論:間充質(zhì)干細胞治療糖尿病的核心治療潛力、挑戰(zhàn)
這項綜述的結(jié)果支持了間充質(zhì)干細胞療法作為輔助治療糖尿病的潛力,尤其強調(diào)了其對2型糖尿病的療效。糖化血紅蛋白(HbA1c)的顯著降低和胰島素需求的減少,凸顯了MSC療法在顯著改善疾病管理方面超越傳統(tǒng)療法的潛力。
疾病類型差異與聯(lián)合策略:在1型糖尿病(T1DM)中,MSC治療的療效差異更為顯著,這反映了潛在的自身免疫病理以及對β細胞再生和免疫調(diào)節(jié)的迫切需求。MSC和HSC的聯(lián)合療法可能帶來更佳的治療效果,但需要仔細考慮相關(guān)風(fēng)險,包括嚴重不良事件。DPP-4抑制劑等藥物在2型糖尿病和神經(jīng)退行性疾病中對免疫調(diào)節(jié)和代謝改善的潛在協(xié)同作用已被探索。
細胞來源優(yōu)先級與發(fā)病機制的關(guān)聯(lián):這些結(jié)果與最近的報告一致,這些報告表明華通膠衍生的MSCs在T2DM中表現(xiàn)出卓越的免疫調(diào)節(jié)和再生能力。最近的評論還強調(diào)了炎癥級聯(lián)(包括NF-κB/NLRP3軸)在糖尿病相關(guān)神經(jīng)退行性疾病和帕金森病合并癥中的病理作用。同樣,淀粉樣蛋白聚集的致糖尿病作用與阿爾茨海默病和T2DM中的重疊通路有關(guān)。
基于MSC來源的療效差異凸顯了對標(biāo)準(zhǔn)化治療方案的迫切需要。沃頓膠衍生的MSCs和BM-MNC的卓越功效表明在未來的臨床試驗中應(yīng)優(yōu)先考慮這些來源。相反,臍帶血衍生的MSCs性能不佳表明在臨床應(yīng)用中應(yīng)謹慎。MSC療法,尤其是使用WJ-MSCs和BM-MNCs的療法,可以作為胰島素抵抗患者的輔助或替代療法。
新興研究表明二甲雙胍可以增強成纖維細胞生長因子21 (FGF21),這是一種可能與MSC通路協(xié)同作用的代謝調(diào)節(jié)劑。然而,在臨床應(yīng)用之前,必須解決生產(chǎn)標(biāo)準(zhǔn)化、交付物流和監(jiān)管障礙。
當(dāng)前干細胞治療糖尿病的轉(zhuǎn)化瓶頸與局限性
當(dāng)前研究存在三大核心局限:
- ①治療方案異質(zhì)性高(細胞制備/給藥方案未標(biāo)準(zhǔn)化);
- ②隨訪期普遍較短(中位≤12個月);
- ③長期安全性證據(jù)匱乏(腫瘤發(fā)生/自身免疫風(fēng)險未明確)。
亟需通過統(tǒng)一生產(chǎn)標(biāo)準(zhǔn)、優(yōu)化遞送系統(tǒng)及建立長期監(jiān)測框架推動臨床轉(zhuǎn)化。
結(jié)論與未來展望
基于對現(xiàn)有高質(zhì)量系統(tǒng)綜述和薈萃分析的整合,本研究表明MSC療法有望成為糖尿病管理(尤其是2型糖尿病)的一種有前景的輔助手段。
特別是源自沃頓膠(WJ-MSCs)或骨髓單核細胞(BM-MNCs)的療法,在治療糖尿病(尤其T2DM)中顯示出顯著改善血糖控制(降低HbA1c)和減少胰島素需求的潛力,且具有可接受的安全性。這為開發(fā)超越傳統(tǒng)胰島素替代的療法帶來了希望。
然而,將其確立為標(biāo)準(zhǔn)臨床療法仍面臨重大挑戰(zhàn):治療方案的高度異質(zhì)性、長期安全性和有效性數(shù)據(jù)的缺乏、以及需要更強大臨床證據(jù)。
未來的研究必須優(yōu)先解決這些瓶頸——應(yīng)優(yōu)先開展大規(guī)模、隨機對照試驗,并采用標(biāo)準(zhǔn)化方案,重點關(guān)注最佳的MSC來源、劑量和給藥方法。超過五年的長期隨訪對于全面評估其持久性和安全性至關(guān)重要。探索MSC介導(dǎo)的免疫和再生途徑的機制研究可以提高治療的精準(zhǔn)度,從而根據(jù)患者的具體特征和糖尿病亞型制定個性化治療方案。
參考資料:[1]:https://www.sciencedirect.com/science/article/abs/pii/S0040816625003234?via%3Dihub
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信