腎病是全球范圍內日益嚴重的健康威脅,據世界衛生組織統計,全球約10%的成年人受其影響,而早期患者中僅少數能得到有效干預。隨著疾病進展,患者將面臨腎功能不可逆損傷、透析依賴甚至死亡的風險。然而,傳統治療手段(如降壓藥、免疫抑制劑)僅能延緩病情發展,無法修復已受損的腎臟組織,這一困境讓無數患者陷入“等待透析或移植”的絕望循環。
近年來,干細胞治療因其獨特的再生與修復能力,為早期腎病患者帶來了新的希望。本文結合多項臨床研究進展與機制探索,系統分析干細胞治療早期腎病的療效、優勢及現存挑戰。
哪些腎病屬于早期腎病范圍呢?
早期腎病主要指腎功能損傷較輕(eGFR≥60ml/min)且病理改變可逆的疾病階段,常見類型包括:
- 原發性腎病:如IgA腎病早期(僅有血尿或少量蛋白尿)、Ⅰ-Ⅱ期膜性腎病、微小病變型腎病(無持續腎損傷);
- 繼發性腎病:如糖尿病腎病微量白蛋白尿期(UACR 30-300mg/g)、高血壓腎病(僅微量蛋白尿)、狼瘡性腎炎Ⅰ-Ⅱ型(無腎小球硬化);
- 急性可逆性腎病:如急性腎小球腎炎(Scr正常)、藥物性間質性腎炎(及時停藥可恢復)。
根據CKD分期,早期腎病涵蓋1期(eGFR≥90)和2期(eGFR 60-89),需結合尿蛋白、血尿或影像學異常綜合判斷。臨床多表現為無癥狀性尿檢異常(尿蛋白<1g/24h)或輕度腎病綜合征(尿蛋白<3.5g/24h)。
需特別關注易快速進展的早期腎病,如局灶節段性腎小球硬化(FSGS)、糖尿病腎病合并血糖失控、多囊腎等,即使eGFR正常也需積極干預。
干細胞治療早期腎病:是延緩進展還是逆轉損傷?
一、干細胞治療早期腎病的作用機制
干細胞(如間充質干細胞、臍帶干細胞)通過以下機制修復腎臟損傷:
1.多向分化與組織修復:干細胞可定向分化為腎小管上皮細胞、血管內皮細胞等,直接替代受損細胞,修復腎臟結構。例如,研究顯示臍帶間充質干細胞(UC-MSCs)在腎小管損傷區域分化為功能細胞,恢復其過濾與重吸收功能。
2.抗炎與抗纖維化:干細胞分泌抗炎因子(如IL-10、TGF-β)和生長因子(如VEGF),抑制炎癥反應,減少腎纖維化進程。
3.免疫調節與歸巢性:干細胞通過調節T細胞亞群平衡,減輕自身免疫損傷;同時,其“歸巢”特性使其精準遷移到腎臟損傷部位,實現靶向修復。
4.促進血管新生:干細胞通過激活內皮祖細胞,促進腎臟微血管再生,改善局部缺血缺氧狀態,從而保護腎功能
二、臨床療效的實證與進展
案例1:間充質干細胞移植治療早期難治性狼瘡性腎炎的長期臨床療效
2014年,南京三甲醫院在行業期刊《Clinical Rheumatology》上發表了一篇關于《異基因間充質干細胞移植治療對常規療法無效的狼瘡性腎炎患者》的研究成果。

本次研究于2007年至2010年進行,共招募了81名中國活動性和難治性狼瘡性腎炎患者(患者大部分處于早期(CKD 1-2期)范圍)。然后在12個月內對所有患者進行監測,并定期進行隨訪,以評估腎臟緩解情況以及可能的不良事件。
在12個月的隨訪中,總生存率為95% (77/81)。總共有60.5% (49/81) 的患者在12個月隨訪期間通過MSCT達到腎臟緩解。
同種異體間充質干細胞移植(MSCT)后,根據不列顛群島狼瘡評估組 (BILAG) 評分評估的腎臟活動性顯著下降(平均值±SD,從基線時的4.48±2.60下降到12個月時的1.09±0.83,表明腎功能明顯改善。
此外治療后,系統性紅斑狼瘡疾病活動指數 (SLEDAI) 評分評估的總體疾病活動度也下降(平均值±SD,從基線時的13.11±4.20到12個月時的5.48±2.77)。 并且,同時服用的潑尼松和免疫抑制藥物的劑量逐漸減少。
綜上所述,間充質干細胞移植對常規治療無效的活動性和難治性狼瘡性腎炎患者(尤其是早期CKD 1-2期)具有顯著療效。12個月隨訪顯示總生存率達95%,60.5%患者實現腎臟緩解,BILAG腎臟評分和SLEDAI疾病活動度顯著下降,同時激素及免疫抑制劑用量減少。這一成果為難治性狼瘡性腎炎提供了新的治療選擇,尤其強調早期干預可有效改善腎功能、延緩疾病進展,并提示間充質干細胞在免疫調節與組織修復中的潛力。
案例2:間充質干細胞對早期糖尿病腎病患者的降糖效果
2021年,汕大二附院聯合花都區人民醫院在行業期刊《干細胞研究與治療》上發表了一篇關于《間充質干細胞在糖尿病腎病中的應用》的薈萃分析。該研究系統納入了29篇文獻中的33項臨床研究,其中幾項臨床研究重點聚焦于干細胞療法對早期糖尿病腎病患者的療效評估,為該療法的臨床應用提供了循證依據。

臨床結果表明:
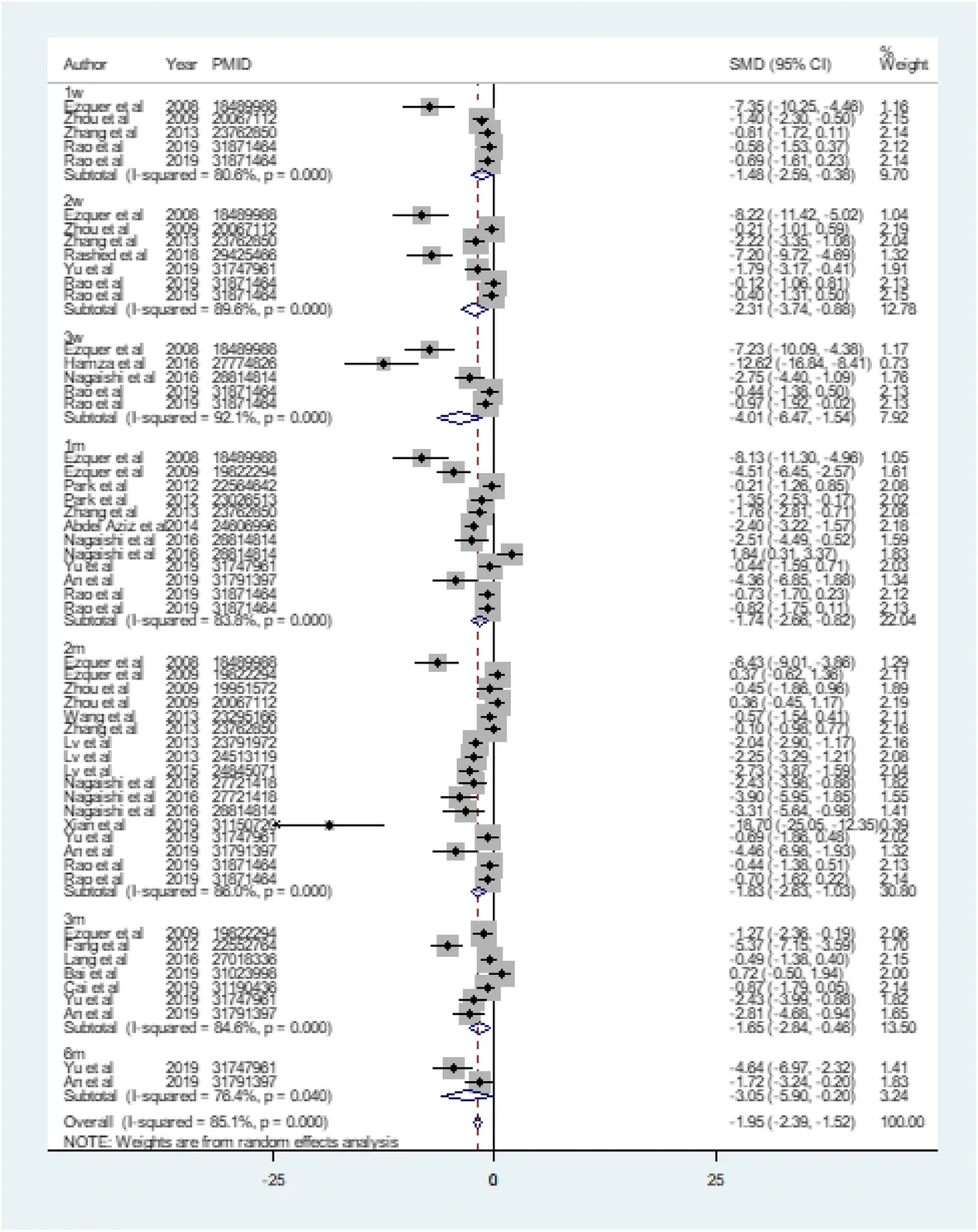
間充質干細胞治療組在第1周、第2周、第3周、第1個月、第2個月、第3個月和第6個月均表現出顯著的降血糖效果,總體降血糖效果顯著。(見圖1)
研究還分析了對血清肌酐 (SCr) 和血尿素氮 (BUN) 的總體影響,表明MSC降低了SCr和BUN,減輕了腎功能損傷。(見圖2.3)
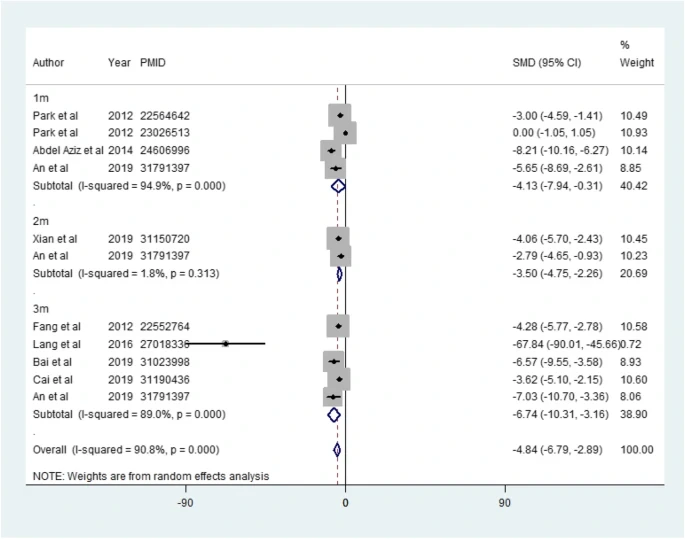
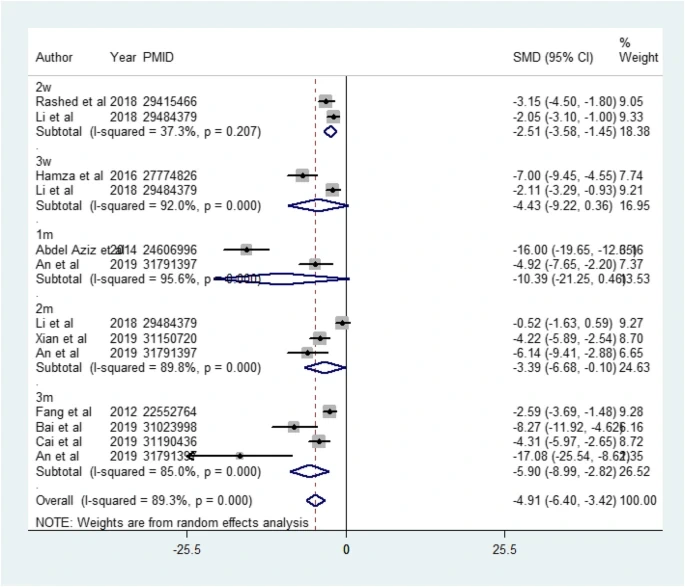
此外,MSC治療減少了尿白蛋白的排泄。對纖維化指標進行了評估,結果顯示與對照組相比,MSC治療組的轉化生長因子-β、膠原蛋白 I、纖連蛋白和α-平滑肌肌動蛋白顯著降低。
綜上所述,本研究為間充質干細胞治療早期糖尿病腎病提供了有力的臨床和機制證據,其多靶點修復作用(降糖、保護腎功能、抑制纖維化)為該疾病的治療開辟了新路徑,具有顯著的臨床轉化價值,在1周到6個月均表現出顯著的降血糖效果,并且減輕了患者腎功能損傷。
案例3:干細胞移植治療早期特殊類型慢性腎病患者的長期預后分析
2024年8月,梅奧診所在期刊《美國血液學雜志》上發表了一篇關于《接受自體干細胞移植的腎AL淀粉樣變性患者的長期結果:驗證腎臟分期系統的性能》的研究成果。
腎AL是指系統性輕鏈(AL)型淀粉樣變性所導致的腎臟損害。根據目前醫學界的共識,腎AL淀粉樣變性可被視為一種特殊類型的慢性腎臟病,因為它通常表現為持續性的腎臟損害和功能下降。

本研究通過回顧性分析2003-2020年697例接受自體干細胞移植(ASCT)的腎AL淀粉樣變性患者數據,評估其長期腎臟預后及腎臟分期系統的預測價值。
根據基線24小時蛋白尿和估算腎小球濾過率(eGFR)水平,患者被分為腎分期I、II、III期。平均隨訪時間為10.4年,腎臟生存率定義為從ASCT到開始腎臟替代治療(RRT)的時間。研究結果顯示:
- 整體情況:大約21%(五分之一)的患者最終發展為嚴重腎衰竭(需要透析或腎移植),平均需要3.4年才會到這個階段;而大部分79%晚期腎衰竭的情況出現在干細胞移植手術后10年以上。
- 腎功能分期影響風險:患者的腎功能分期(I期最輕,III期最重)直接影響未來需要透析或腎移植的可能性。具體來說:
- I期患者:3年內僅有3%的概率需要透析或移植;
- II期患者:概率上升到10%;
- III期患者(病情最重):3年內的風險高達37%。
綜上所述,干細胞治療在早期腎病領域展現出顯著潛力,通過再生修復與抗纖維化機制改善腎功能、延緩腎衰竭進展(大部分早期腎病患者能延緩10年以上)。并且腎臟分期是一個可靠的工具來評估患者的預后,這些信息可以幫助醫生制定更有效的個體化治療策略,以提高患者的生存質量并延長生存時間。
干細胞治療早期腎病患者療效總結
綜上所述,干細胞治療在早期慢性腎臟病(CKD 1-2期)中展現出顯著潛力,尤其對傳統治療無效的難治性腎病(如狼瘡性腎炎、糖尿病腎病、腎AL淀粉樣變性等)具有突破性療效。
研究顯示,間充質干細胞(MSC)或自體干細胞移植可顯著改善腎功能:例如,狼瘡性腎炎患者60.5%實現腎臟緩解,BILAG腎臟評分和疾病活動度顯著下降;糖尿病腎病患者血糖、血清肌酐及尿蛋白水平改善,纖維化進程被抑制;腎AL淀粉樣變性早期患者腎衰竭進展延緩超10年。其療效源于干細胞的多靶點作用,包括抗炎、免疫調節、抗纖維化及組織再生,同時減少對激素和免疫抑制劑的依賴。
并且干細胞治療的早期干預優勢尤為突出,早期腎病患者對治療反應更佳,顯著延緩終末期腎病(ESRD)發生,且安全性較高(如狼瘡性腎炎12個月生存率達95%)。
三、為何早期干預效果會更佳呢?
研究表明,干細胞治療的臨床效果與腎病階段密切相關,其修復能力在早期腎病中表現顯著,而在晚期腎病中則受限于腎臟結構的不可逆損傷,但仍可延緩疾病進展。
早期干預效果更佳的核心原因
- 病理損傷可逆性強:早期腎病腎組織損傷較輕(如eGFR≥60、纖維化面積<10%),干細胞能直接修復凋亡細胞并再生腎單位(如足細胞、內皮細胞),逆轉率比晚期高3-5倍。
- 炎癥與纖維化可控:早期炎癥因子(TNF-α、IL-6)水平低,干細胞通過分泌抗炎因子(IL-10)快速抑制免疫攻擊;同時阻斷TGF-β/Smad通路,有效延緩膠原沉積,避免纖維化“不可逆網絡”形成。
- 干細胞活性更高:早期腎臟趨化因子(SDF-1)豐富,干細胞歸巢率達60%-70%,且健康微環境保障其旁分泌功能(如外泌體miR-21),促進血管新生和代謝廢物清除;晚期因纖維化屏障,歸巢率驟降至20%-30%。
- 避免惡性循環:早期干預可阻斷高血壓、高血糖等繼發損傷,防止腎小球基底膜持續破壞;年輕患者(<40歲)因細胞再生能力強,修復速度比老年患者快2-3倍。
總結:早期腎病存在“黃金時間窗”,干細胞在結構完整、微環境未惡化時修復效率最高;一旦進入晚期(eGFR<30),纖維化與代謝毒性將大幅削弱療效,因此早篩早治是關鍵。
四、當前挑戰與未來方向
1.主要挑戰
技術標準化缺失:干細胞來源(骨髓、臍帶)、制備流程及輸注途徑(靜脈、動脈內)尚未統一,影響結果可重復性。
技術瓶頸:干細胞歸巢效率、個體化劑量方案仍需優化。
2.未來方向
聯合治療:結合基因編輯(如CRISPR)增強抗纖維化功能,或與納米載體結合提高靶向性。
早期干預:推廣定期篩查(尿常規、血肌酐),把握治療窗口期。
結語
干細胞治療為早期腎病患者提供了“修復而非替代”的新思路,尤其在改善腎功能指標、延緩纖維化方面表現突出。隨著遞送技術和標準化方案的推進,其有望成為腎病管理的核心手段。但是,患者需在專業醫療機構評估病情分期及個體適應性,以最大化獲益。
參考資料:
Gu, F., Wang, D., Zhang, H. et al. Allogeneic mesenchymal stem cell transplantation for lupus nephritis patients refractory to conventional therapy. Clin Rheumatol 33, 1611–1619 (2014). https://doi.org/10.1007/s10067-014-2754-4
Lin, W., Li, HY., Yang, Q. et al. Administration of mesenchymal stem cells in diabetic kidney disease: a systematic review and meta-analysis. Stem Cell Res Ther 12, 43 (2021). https://doi.org/10.1186/s13287-020-02108-5
Muchtar E, Gertz MA, Mwangi R, et al. Long-term outcomes of renal AL amyloidosis patients undergoing autologous stem cell transplantation: Validating the performance of the renal staging system. Am J Hematol. 2024; 99(11): 2118-2126. doi:10.1002/ajh.27460
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信