糖尿病已成為一種流行病,影響著全球超過5.89億人,導致他們終生需要服藥。糖尿病是導致失明、腎衰竭、心臟病發作和中風的主要原因。預計到2050年,受糖尿病影響的人數將上升到8.53億。生物技術正在努力尋找能夠治愈這種慢性疾病的糖尿病治療方法,但我們離目標還有多遠?
糖尿病治療的未來:有可能治愈嗎?
盡管糖尿病對全球人口影響巨大,但目前任何類型的糖尿病都無法治愈。大多數治療方法在一定程度上幫助患者控制癥狀,但糖尿病患者仍然面臨多種長期健康并發癥。
糖尿病會影響胰島素(一種細胞吸收葡萄糖所需的激素)的調節,導致血糖水平升高。雖然癥狀有些相似,但兩種主要的糖尿病類型發展方式不同。
1型糖尿病是一種自身免疫性疾病,會破壞產生胰島素的β胰腺細胞。相比之下,2型糖尿病患者會產生胰島素抵抗,這意味著胰島素降低血糖的效果越來越差。?
盡管世界衛生組織 (WHO) 等組織僅正式認可1型和2型糖尿病,但研究人員已提出其他亞型,以更好地反映糖尿病病例的多樣性。例如,3c型糖尿病是指由胰腺損傷引起的病例,而3型糖尿病則用于描述與腦部胰島素抵抗相關的阿爾茨海默病,盡管存在爭議。4型和5型糖尿病最近出現在科學文獻和媒體中,分別用于描述體型偏瘦人群的年齡相關性糖尿病和年輕人的營養不良相關性糖尿病。這些術語尚未得到官方認可,但它們體現了人們為更好地理解該疾病非典型形式所做的努力。
讓我們看看該領域正在發生什么以及它將如何改變糖尿病的治療方式。
目錄
- 1型糖尿病治療
- 2型糖尿病治療
- 糖尿病治療的下一步是什么?
1型糖尿病治療
治愈糖尿病的斗爭可以追溯到1921年,當時胰島素被發現。從那時起,我們對這種疾病有了更多的了解,生物科技公司也嘗試了多種方法,其中一些方法比其他方法更成功。
1型糖尿病簡史
1921/1922–發現胰島素并首次注射胰島素
弗雷德里克·班廷和查爾斯·貝斯特分離出胰島素,為糖尿病的治療奠定了基礎。倫納德·湯普森成為首位接受胰島素治療的患者。
1959年——糖尿病類型的區分
科學家區分了 1 型和 2 型糖尿病,從而可以制定更有針對性的研究和治療策略。
1982年——首個合成人胰島素獲批
Humulin成為第一種基因工程人類胰島素,提高了純度并減少了過敏反應。
2016年——FDA批準首個混合閉環系統
美敦力公司的 MiniMed 670G成為美國食品藥品監督管理局 (FDA) 批準的首個“人工胰腺”系統,可根據持續血糖監測自動調整胰島素輸送。
2022年——首個改善病情的藥物獲批(Teplizumab)
FDA批準 Tzield,這是第一種被證實可以延緩高危人群患上1型糖尿病的藥物。
2024年——首次報道通過干細胞療法實現胰島素依賴性
中國一名患者在接受干細胞來源的胰島細胞移植后實現了胰島素依賴。
利用人工胰腺治療疾病
1 型糖尿病的管理已經有了顯著的進步,已經從傳統的胰島素注射轉向更加自動化和精確的輸送方法。
現代胰島素泵可持續皮下輸注胰島素,比每日多次注射更能穩定血糖控制。近期的創新包括貼片泵和無管系統,提高了患者的便利性和自主性。
最具變革意義的進步之一是混合閉環系統的開發,通常被稱為人工胰腺的早期形式。這些系統集成了持續血糖監測 (CGM)、胰島素泵和先進的算法,可實時自動調整胰島素輸送,旨在將血糖水平維持在目標范圍內,并減輕持續人工監測的負擔。
值得關注的例子包括美敦力的MiniMed 670G,該產品于2016年獲得FDA批準。它是首個混合閉環系統,可根據CGM讀數自動調整基礎胰島素輸送。Tandem t:slim X2配備Control-IQ系統,并結合預測算法來微調胰島素輸送,從而改善治療效果。
智能胰島素(Smart Insulin)的研究也在不斷推進,這是一種葡萄糖反應性胰島素制劑,僅在血糖水平升高時啟動。早期動物模型研究已顯示出良好的前景,如果這些方法成功應用于人類治療,有望降低低血糖風險并簡化胰島素治療。
利用免疫療法攻擊病源
由于1型糖尿病是一種自身免疫性疾病,最有前景的研究方向之一是阻止或至少減緩免疫系統對產生胰島素的β細胞的攻擊。越來越多的療法正在接受測試,以延緩疾病發作或保留剩余的β細胞功能,尤其是在疾病的早期階段。
2022年,FDA批準了teplizumab(商品名Tzield),使其成為首個專門用于延緩臨床1型糖尿病發作的藥物。該藥物是一種抗CD3單克隆抗體,有助于調節參與自身免疫攻擊的T細胞活性。臨床研究表明,接受teplizumab治療的糖尿病高危人群比未接受治療的人群平均多維持兩年無糖尿病狀態。
另一種正在研究中的方法是,以受控的方式引入β細胞抗原(通常存在于胰島素分泌細胞中的蛋白質),以“教導”免疫系統不要攻擊它們。在一項早期試驗中,研究人員在近期確診的患者身上使用了六種β細胞肽的混合物,并觀察到免疫調節恢復的跡象。
一些實驗室也在研究改造免疫細胞,例如耐受性樹突狀細胞,以幫助重新訓練免疫系統。這些工程細胞可以促進調節性T細胞的產生,從而抑制自身免疫攻擊。該概念尚處于早期階段,但初步臨床試驗表明,這種細胞療法是安全的,值得進一步探索。
除了靶向免疫療法外,研究人員還在重新利用更廣泛的免疫調節藥物。用于治療類風濕性關節炎的JAK抑制劑巴瑞替尼,在近期確診為1型糖尿病的患者中顯示出令人鼓舞的效果。與未接受治療的患者相比,接受該藥物治療的患者需要的胰島素更少,并且β細胞功能保持得更好。
用細胞療法替代缺失的細胞:干細胞治療1型糖尿病
恢復1型糖尿病患者胰島素分泌的嘗試越來越多地集中在再生療法上,尤其是基于干細胞的療法。其目的是替換被破壞的胰腺β細胞或保護它們免受損害。
2024年,細胞療法取得了對抗糖尿病的最大勝利之一。中國的一個案例表明,一位25歲的1型糖尿病女性在接受源自自身重編程干細胞的胰島樣細胞移植后,實現了胰島素依賴。這些細胞被植入她的腹部肌肉,三個月內,她就不再需要注射胰島素了。這一結果表明,自體干細胞療法有可能在無需免疫抑制的情況下恢復內源性胰島素的產生。
雖然這一成功意義重大,但使用自身細胞難以規模化和商業化。為此,Vertex Pharmaceuticals 一直在開發 VX-880,這是一種利用源自人類胚胎干細胞的完全分化胰島細胞的療法。在試驗中,一些參與者在接受這種將細胞輸注到肝門靜脈的治療后實現了胰島素依賴。雖然這種方法前景光明,但目前需要免疫抑制治療來防止排斥反應。
為了避免免疫抑制治療,研究人員正在探索封裝裝置,以保護移植的胰島細胞免受免疫攻擊,同時允許葡萄糖和胰島素通過。例如,ViaCyte的PEC-Encap裝置將胰腺祖細胞封裝在半透膜內。早期試驗表明,一些患者的血糖控制得到改善,而無需全身免疫抑制治療。
隨著研究的推進,監管機構的批準也開始陸續到來。2023年,FDA批準了donislecel(Lantidra),這是首個針對1型糖尿病成人嚴重低血糖患者的同種異體胰島細胞療法。該療法源自已故捐贈者的胰腺,將胰島細胞注入肝臟。在臨床研究中,相當一部分接受者在不同時間實現了胰島素依賴。

利用基因編輯克服細胞治療的挑戰
細胞療法面臨的主要挑戰之一是,新植入的胰島素分泌細胞通常會被免疫系統識別并摧毀,而這正是最初導致疾病的機制。研究人員目前正在利用基因編輯技術,幫助這些細胞不被免疫系統發現。
例如,CRISPR Therapeutics 和 Vertex Pharmaceuticals最初合作研發 VCTX210A,這是一種基因編輯的同種異體干細胞衍生療法,用于治療1型糖尿病。然而,Vertex于2024年初決定終止合作。因此,CRISPR Therapeutics完全擁有該項目,并將其更名為CTX-211。這款新的候選藥物包含額外的基因編輯,旨在增強細胞適應性和免疫逃避能力。CTX-211 的一期臨床試驗目前正在進行中。?
另外,Vertex繼續開發自己的1型糖尿病療法,例如VX-880和VX-264。
2型糖尿病治療
2型糖尿病占全球糖尿病病例的絕大多數,其主要原因是胰島素抵抗和進行性β細胞功能障礙。雖然改變生活方式仍然是預防和早期管理的基石,但過去幾十年來,生物制藥的選擇已顯著擴展。
2型糖尿病簡史
1959年——糖尿病類型的區分
美國糖尿病協會正式區分 1 型糖尿病和 2 型糖尿病,認識到它們的不同病因和治療需求。?
1995年–美國食品藥品監督管理局 (FDA) 批準二甲雙胍在美國上市
在歐洲使用多年后,二甲雙胍獲得 FDA 批準,成為美國2型糖尿病的一線治療藥物。?
2005年-艾塞那肽(Byetta)獲批
FDA 批準了首個 GLP-1 受體激動劑艾塞那肽,從而引入了一類可增強胰島素分泌和抑制胰高血糖素釋放的新型注射藥物。?
2006 年–西他列汀(Januvia)獲批
西他列汀是首個 DPP-4 抑制劑,已獲批準,它是一種口服藥物,可提高腸促胰島素水平,從而改善血糖控制。?
2012 年–卡格列凈(Invokana)獲批
卡格列凈成為 FDA 批準的第一個 SGLT2 抑制劑,通過促進尿糖排泄提供了一種降低血糖的新機制。?
2017年——司美格魯肽 (Ozempic) 獲批
每周一次的 GLP-1 受體激動劑索馬魯肽已獲批準,在血糖控制和減肥方面顯示出顯著的益處。?
2022年——tirzepatide(Mounjaro)獲批
Tirzepatide 是一種雙重 GIP 和 GLP-1 受體激動劑,已獲批準,與現有療法相比,它具有增強的血糖控制和減肥功效。
2025年——預計奧格列酮獲批
禮來公司的口服GLP-1受體激動劑 orforglipron的3期試驗結果令人鼓舞,有可能成為首個有效的2型糖尿病口服GLP-1療法。
刺激胰島素分泌
2 型糖尿病治療的最大轉變之一是胰高血糖素樣肽 1 (GLP-1) 受體激動劑的出現,它可以刺激胰腺 β 細胞產生胰島素并抑制胰高血糖素的分泌。?
GLP-1激動劑最初被開發用于控制血糖,但在2023年,研究強調了其對肥胖和心臟病患者的益處,使其獲得了巨大的關注。一項美國試驗涉及529名接受索馬魯肽治療糖尿病和Wegovy(索馬魯肽)治療肥胖癥的患者,參與者在接受一年治療后心臟狀況改善了一倍。另一項涉及1.7萬人的大規模研究發現,服用索馬魯肽的患者患心臟病和中風的可能性降低了20%。
新一代聯合療法正在進一步提升這些益處。Tirzepatide(Mounjaro)于2022年獲批,它將GLP-1和抑胃肽(GIP)的作用整合在一個分子中。這種雙重作用有助于降低血糖水平、減少食欲并促進脂肪減少。該藥物也于2023年以Zepbound的商品名獲批,用于非糖尿病患者的體重管理。
更有雄心勃勃的候選藥物正在研發中。研究人員目前正在測試結合GLP-1、GIP和胰高血糖素受體活性的三重激動劑,以通過增加能量消耗來進一步增強減肥效果。
藥物輸送也在不斷發展。GLP-1 傳統上需要注射,但口服制劑即將問世。禮來公司 (Eli Lilly) 的口服GLP-1受體激動劑 Orforglipron在 2025 年的 III 期臨床試驗中取得了令人鼓舞的結果,并可能很快為患者提供無針治療選擇,從而有助于提高患者的長期依從性。
定價仍然是一個障礙,像司美格魯肽這樣的藥物在許多市場每月的費用仍在1000美元左右。更廣泛的可及性可能取決于政策轉變和未來的仿制藥。
針對微生物組
在過去十年中,科學家們已經意識到我們體內和體表的微生物對我們的健康起著重要作用。人體微生物群,尤其是腸道微生物群,與多種慢性疾病有關,包括糖尿病。
最近的研究探索了旨在調節腸道菌群以改善血糖控制的干預措施。例如,糞便菌群移植 (FMT) 已被研究作為一種恢復腸道菌群平衡的方法。《自然》雜志 2024 年的一篇綜述指出,雖然 FMT 可以改變腸道菌群組成,但其在改善2型糖尿病患者胰島素敏感性方面的長期療效仍不確定,這凸顯了進一步研究標準化方案和供體選擇的必要性。
Pendulum Therapeutics 開發了“Pendulum Glucose Control”,這是一款醫用益生菌,含有Akkermansia muciniphila和Clostridium butyricum等菌株。臨床研究表明,該配方可使 2 型糖尿病患者的糖化血紅蛋白 (A1c) 水平降低0.6%,餐后血糖峰值降低 33%。?
最近,Valbiotis公司的TOTUM-63(一種富含植物多酚的提取物)在治療早期2型糖尿病方面顯示出良好的前景。在2024 年歐洲糖尿病研究協會 (EASD) 年會上公布的一項2/3期臨床研究表明,TOTUM-63顯著降低了糖尿病前期和早期2型糖尿病患者的糖化血紅蛋白水平。
雖然這些進展令人鼓舞,但腸道微生物組的復雜性及其與宿主代謝的相互作用仍需進一步研究。確定因果關系并理解這些干預措施背后的機制,對于將微生物組靶向療法整合到標準的2型糖尿病管理方案中至關重要。
干細胞治療2型糖尿病
近年來,干細胞治療在2型糖尿病領域逐漸從實驗室走向臨床探索,吸引了不少關注。我們都知道,2型糖尿病的核心問題在于身體對胰島素的利用效率下降(胰島素抵抗),以及生產胰島素的β細胞功能逐漸衰退甚至數量減少。現有的藥物和胰島素注射雖然能有效控制血糖,但更像是“管理”而非“根治”,而且需要長期堅持,部分患者還會面臨低血糖等風險。
干細胞,尤其是間充質干細胞(MSCs),之所以被看好,主要是它們展現出的幾方面潛力:一是修復能力。一些研究發現,這些細胞可能有助于改善受損的胰島β細胞功能,或者促進其再生,相當于給“疲憊的胰島素工廠”加把勁。二是調節免疫和炎癥。2型糖尿病常常伴隨著慢性低度炎癥,而干細胞具有調節免疫反應、減輕炎癥環境的作用,這恰恰可能改善胰島素抵抗的問題。三是促進血管新生。良好的血管供應對胰島功能至關重要,干細胞可能幫助改善胰島局部的微循環。
目前的研究進展如何呢?確實有一些小規模的臨床研究(主要是I/II期)結果令人鼓舞。比如:
2024年5月,首例自體再生胰島治愈T2DM:上海長征醫院利用患者血液PBMC重編程為iPSC,再分化為胰島組織移植。一名25年病史患者術后11周完全停胰島素,血糖穩定33個月,C肽持續恢復。
2025年6月,解放軍總醫院聯合南開大學醫學團隊發布的一項權威研究成果表明,臍帶間充質干細胞(UCMSC)輸注治療不僅能幫助患者實現血糖穩定達標,還能顯著逆轉脂肪肝,脂肪肝逆轉率高達46%!這一項研究為代謝性疾病的綜合干預提供了嶄新思路,也為患者帶來了振奮人心的希望。

1.修復胰島功能,穩定血糖:UCMSC療法通過釋放活性因子,修復受損的胰島細胞功能,同時增強機體對胰島素的敏感性,顯著降低胰島素抵抗。這使患者能夠更高效地控制血糖水平,減少因血糖波動導致的并發癥風險。
2.血糖達標率顯著提高:UCMSC治療組患者的糖化血紅蛋白(HbA1c)水平顯著降低,并有更多患者將血糖控制在理想范圍(<7%)。與對照組相比,干細胞治療的效果更加突出,顯示了這一療法在控糖方面的強大潛力。
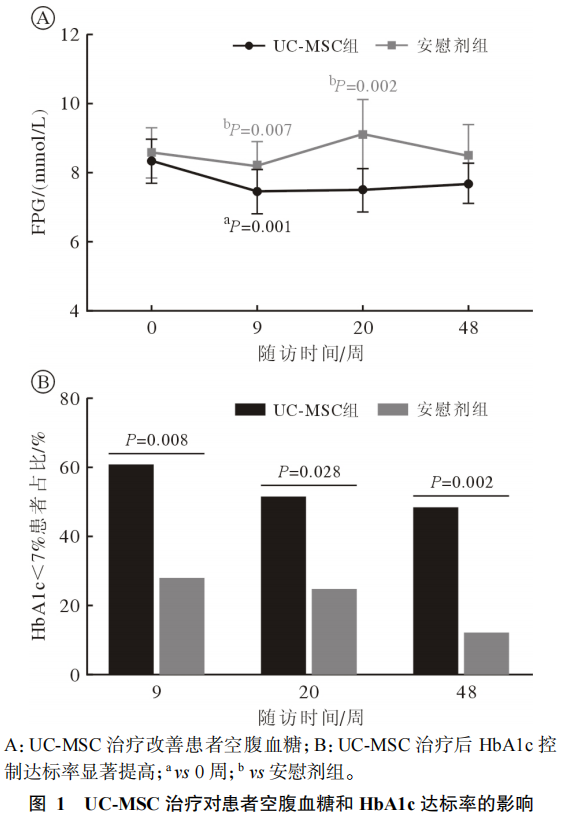
但是,咱們也得冷靜看待。?干細胞治療2型糖尿病遠未成熟,還處在研究的“青春期”。
幾個關鍵問題依然懸而未決:效果能持續多久??目前觀察到的改善大多是幾個月到一兩年,長期效果需要更大規模、更長隨訪的研究來確認。最佳的治療方案是什么??用哪種干細胞?輸多少量?通過什么途徑(靜脈、胰腺局部等)?多久輸一次?這些都還沒有標準答案。作用機制究竟如何??干細胞是直接變成了新的β細胞?還是主要通過分泌各種有益因子(旁分泌效應)來調節微環境、修復損傷?這背后的原理還需要更深入的探究。最后,也是最重要的,大規模應用的安全性和長期風險,還需要更嚴格的III期臨床試驗來充分評估。
總的來說,干細胞治療為2型糖尿病患者帶來了新的希望和可能性,初步的臨床結果也顯示出了一定的療效和安全性。它代表著一種潛在的新型治療策略,目標不僅僅是控制血糖,更是試圖去解決疾病的根本病理生理問題。然而,從充滿希望的實驗室數據和早期臨床試驗,到真正成為一種被廣泛認可、安全有效的常規治療手段,還有很長的科學和監管之路要走。
科研人員正在努力攻關,未來幾年更大規模、設計更嚴謹的臨床試驗結果,將為我們描繪更清晰的圖景。這是一個充滿活力但也需要耐心的研究領域,在現實與希望之間,科學正在穩步前行。
糖尿病治療的下一步是什么?
在1型糖尿病中,細胞療法已開始展現出改變生命的潛力。但新的努力正致力于使這些療法更具可擴展性和可及性,包括開發能夠逃避免疫攻擊的基因編輯胰島素分泌細胞,以及無需免疫抑制即可保護其免受排斥的裝置。延緩或預防1型糖尿病發作的免疫調節策略也越來越受到關注,將目標從治療轉向預防。
2型糖尿病的下一波浪潮或許并非由單一藥物決定,而是由多種技術的融合所決定。智能胰島素、納米技術口服給藥以及無創血糖監測工具正在開發中,以減輕治療負擔。研究人員也在研究早期干預策略,包括針對腸道的治療、微生物組調節和代謝重編程,以便在疾病進展之前將其控制住。
在這兩種類型的疾病中,人工智能正越來越多地被用于個性化治療方案、實時風險監測和優化劑量。隨著對糖尿病的理解不斷加深,代謝、免疫和內分泌途徑之間的區別也變得越來越模糊。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信