糖尿病是威脅人類健康的主要慢性疾病之一,其中1型糖尿病(T1D)由自身免疫攻擊導致胰島β細胞功能衰竭,患者血糖波動劇烈。長期依賴胰島素注射,不僅容易出現嚴重低血糖、腎功能衰竭、視網膜病變等并發癥,還極大影響生活質量。
據世界衛生組織(WHO)統計,我國T1D患兒每年平均需注射胰島素約2000針,預期健康壽命可能縮短高達32年。可以說,胰島素雖能“救命”,卻無法從根本上解決胰島功能喪失問題。
正是在這樣的背景下,干細胞療法,尤其是間充質干細胞療法,為T1D患者帶來了全新的希望。

一、1型糖尿病的發病機制
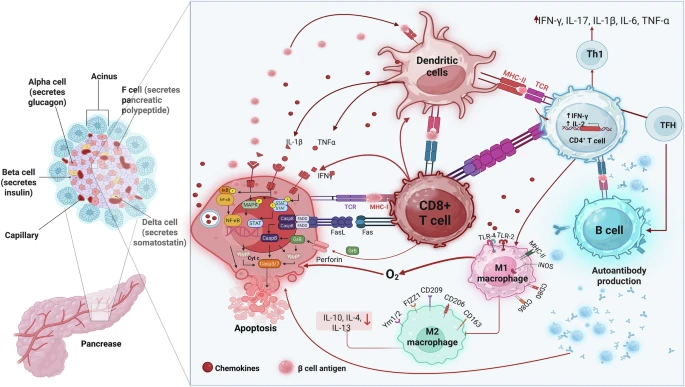
1型糖尿病(T1D)是一種由自身免疫反應引起的慢性疾病,患者的免疫系統錯誤地攻擊并破壞胰島β細胞,導致胰島素分泌不足,從而出現高血糖并需終身依賴胰島素。其發病過程可分為三個階段:
第一階段,免疫悄然啟動:這時血糖還正常,但體內已經出現針對胰島的自身抗體。樹突狀細胞開始聚集到胰島內,免疫系統被輕度激活,β細胞功能已出現早期損傷。
第二階段,免疫系統全面攻擊:隨著免疫反應加劇,T細胞和巨噬細胞釋放炎癥因子,直接攻擊并破壞β細胞,炎癥反應不斷放大。
第三階段,β細胞衰竭:長期炎癥導致氧化應激和內質網應激增強,β細胞大量死亡,胰島素分泌功能幾乎完全喪失,患者進入臨床糖尿病階段。
二、什么是間充質干細胞療法?它為何能修復胰島?
間充質干細胞(MSC)是一類存在于骨髓、臍帶、脂肪等組織的成體干細胞,具有自我復制、多向分化及免疫調節能力。
在T1D治療中,MSC通過兩大核心機制發揮作用——免疫調節和胰島修復,直擊疾病的根源。
1.免疫調節功能:重塑機體免疫平衡
間充質干細胞(MSCs)能通過分泌信號分子和外泌體來調節免疫系統,幫助身體恢復平衡。它們可以抑制過度活躍的免疫細胞,減少炎癥反應,同時增加具有保護作用的Treg細胞數量。這樣一來,胰島β細胞不再被免疫系統“誤傷”,為功能恢復創造條件。
2.促進胰島修復:激活再生與保護機制
除了調節免疫,MSCs還能分泌多種生長因子,促進血管生成、改善胰島的營養供給,并減輕氧化損傷。這些作用能讓胰島細胞在移植或再生過程中更好地存活和工作,從而逐步恢復胰島功能、穩定血糖水平。
正是憑借這些獨特的生物學特性,MSC成為1型糖尿病“功能性治愈”的重要方案之一。
三、2025:間充質干細胞治療1型糖尿病的最新現狀
進入2025年,間充質干細胞療法治療1型糖尿病的研究正在全球范圍內快速推進。多項臨床試驗結果顯示,這一療法不僅能改善患者的血糖控制,還在部分病例中顯現出恢復胰島功能的跡象。
在國內,上海長征醫院等科研團隊已啟動針對自體與異體MSCs的臨床研究,探索其在免疫調節與胰島功能修復中的長期療效;而在國際上,美國、瑞典等國家的研究也相繼證實,靜脈輸注或局部注射MSCs可明顯降低胰島素依賴、減少低血糖事件。
值得關注的是,部分試驗進入中后期階段,患者的隨訪時間已超過兩年,仍能維持穩定的血糖水平。這意味著,MSCs治療正從“輔助性療法”逐漸向“功能性治愈”方向邁進。
雖然目前尚未實現完全替代胰島素,但其安全性與持續療效,已為1型糖尿病的長期管理帶來新的希望。
四、臨床進展與療效數據
臨床案例1:臍帶間充質干細胞治療顯著改善血糖與胰島素依賴
2025年2月4日,埃及本哈大學醫學院在期刊《Expert Review of Endocrinology & Metabolism》上發表了一篇關于”臍帶間充質干細胞治療1型和2型糖尿病的安全性和有效性:系統評價和薈萃分析“的研究成果。[1]

檢索PubMed、Cochrane、WOS、Embase和Scopus數據庫中截至2024年1月關于UCMSCs治療1型和2型糖尿病的隨機對照試驗(RCT)。共納入334例患者(172例實驗組和162例對照組)的8個CT。
基于8項對照試驗(共334例患者)的系統性分析顯示,間充質干細胞(MSCs)在1型糖尿病(T1DM)治療中展現出顯著療效:
1.糖化血紅蛋白(HbA1c)顯著下降
- MSCs組與安慰劑組相比,HbA1c平均差異為?1.24%(95% CI [?1.6, ?0.89],p < 0.00001),表明MSCs能有效改善血糖控制。
- 亞組分析顯示,6項針對T1DM的研究均支持這一結論,且研究間無顯著異質性(I2 = 0%)。
2.胰島素需求量顯著減少:MSCs組每日胰島素需求量平均減少0.24 U/kg/d,提示MSCs可能部分恢復胰島功能,降低外源性胰島素依賴。
3.空腹C肽水平變化整體分析顯示MSCs組與安慰劑組空腹C肽水平差異無統計學意義,但亞組分析發現部分研究顯示MSCs可輕微提升C肽水平,表明其可能促進殘存β細胞功能或新生β細胞生成。
研究表明,MSCs治療1型糖尿病在降低HbA1c、減少胰島素用量方面具有明確優勢,部分研究提示其可能改善β細胞功能,但對C肽的影響仍需更大樣本驗證。
臨床案例2:多國聯合研究證實MSC療法可持續改善血糖控制與胰島功能
2025年6月3日,利比亞米蘇拉塔國家癌癥研究所牽頭在《糖尿病與代謝綜合征》雜志上發表了一篇名為”間充質干細胞治療1型和2型糖尿病:隨機對照試驗的系統評價和薈萃分析“的研究成果。[2]

本綜述回顧并分析了13項RCT,共涉及507名受試者。其中,我國進行了5項研究,印度進行了3項研究,伊朗進行了 2項研究,瑞典進行了2項研究,美國進行了1項研究。
研究觀察到糖尿病患者的糖化血紅蛋白 (HbA1c)、前血糖 (PPBG) 和胰島素需求量在接受干細胞治療六個月和十二個月后持續顯著降低。空腹C肽水平(可指示β細胞功能和基線胰島素分泌)在兩種類型的患者中在12個月的隨訪后也顯著升高。
在半年和一年的隨訪中,T1DM亞組分析顯示HbA1c和胰島素劑量也有所降低。該亞群的 FCP 僅在 12 個月的隨訪中顯著增加。
兩組間空腹血糖(FBG)無顯著差異,但干預組在治療后3、6和12個月的空腹血糖持續較低。此外,MSC療法在改善刺激后C肽、胰島素抵抗指數(HOMA-IR)和HOMA-B指標方面未見明顯效果。
臨床案例3:脂肪間充質干細胞在1型糖尿病治療中展現再生與免疫雙重療效
2025年7月23日,丹麥哥本哈根斯蒂諾糖尿病中心牽頭在國際期刊《nature》上發表了一篇名為“脂肪來源間充質干細胞在1型糖尿病治療中的應用”的臨床應用成果。[3]
本文綜述了脂肪組織來源的間充質干細胞(ADMSCs)療法在治療T1D方面的最新進展和研究成果。

研究發現,ADMSCs不僅能分化為胰島素分泌樣細胞,促進胰島β細胞再生,還能通過分泌多種生長因子(如VEGF、FGF、IGF-1等)改善胰腺微環境,降低血糖、提高胰島素水平和C肽水平,從而改善糖代謝異常。
與骨髓或臍帶來源的干細胞相比,ADMSCs在促進血管生成、調節炎癥反應和維持細胞活性方面表現更優。
此外,ADMSCs在免疫調節方面同樣發揮關鍵作用。它們能抑制促炎細胞因子(如TNF-α、IL-6、IFN-γ)的產生,促進抗炎細胞因子(如IL-10、TGF-β)的分泌,并誘導Treg細胞擴增,從而減輕對β細胞的自身免疫攻擊。研究表明,ADMSC移植可降低T1D動物模型的空腹血糖,恢復胰島結構并延緩病程。
憑借其再生、抗炎及免疫調控三重作用,ADMSCs正成為T1D細胞治療的重要方向,顯示出延緩甚至逆轉病情的潛力。
五、挑戰與未來方向
盡管間充質干細胞療法在1型糖尿病治療中展現出良好的臨床前景和初步療效,但仍面臨一些挑戰:
- 療效穩定性:不同患者對MSC治療的反應存在差異,部分患者隨訪后療效減弱,需要進一步優化治療方案。
- 治療方案標準化:MSC的來源、劑量、給藥途徑和頻次尚無統一標準,需要更多臨床研究指導。
未來方向包括開發高活性MSC、優化移植方案、開展大樣本長期隨訪,以及探索MSC與其他治療手段的聯合應用,以實現更持久的胰島功能恢復。
結語
間充質干細胞療法為1型糖尿病的治療帶來了前所未有的希望。它不僅可以通過免疫調節減輕自身免疫攻擊,還能促進胰島β細胞修復與功能恢復,為患者提供“功能性治愈”的可能性。
盡管當前仍存在療效個體差異、長期穩定性和安全性等挑戰,但隨著研究的深入和技術的進步,MSC療法有望成為未來1型糖尿病管理的核心手段。通過不斷優化治療方案、明確機制及開展多中心臨床驗證,干細胞療法有望真正改變T1D患者的生活質量,讓“血糖管理被動依賴胰島素”向“胰島功能部分恢復”轉變。
參考資料:
[1]Nada AH, Ibrahim IA, Oteri V, Shalabi L, Asar NK, Aqeilan SR, Hafez W. Safety and efficacy of umbilical cord mesenchymal stem cells in the treatment of type 1 and type 2 diabetes mellitus: a systematic review and meta-analysis. Expert Rev Endocrinol Metab. 2025 Mar;20(2):107-117. doi: 10.1080/17446651.2025.2457474. Epub 2025 Feb 4. PMID: 39905688.
[2]Kashbour M, Abdelmalik A, Yassin MNA, Abed M, Aldieb E, Abdullah DM, Elmozugi T, Isawi Y, Hassan E, Almuzghi F. Mesenchymal stem cell-based therapy for type 1 & 2 diabetes mellitus patients: a systematic review and meta-analysis of randomized controlled trials. Diabetol Metab Syndr. 2025 Jun 3;17(1):189. doi: 10.1186/s13098-025-01619-6. PMID: 40462158; PMCID: PMC12131437.
[3]Sood, V., Ricioli, H., Njoku, G.C. et al. Adipose-derived mesenchymal stromal/stem cells in type 1 diabetes treatment. Commun Biol 8, 1094 (2025). https://doi.org/10.1038/s42003-025-08244-z
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信