間充質干細胞(MSCs)作為再生醫學領域的明星細胞,因其獨特的生物學特性——強大的自我更新能力、多向分化潛能、免疫調節功能及分泌多種生物活性因子的能力,成為腦性癱瘓(Cerebral Palsy, CP)治療的前沿突破點。近年來,大量臨床試驗和基礎研究證實,MSCs可通過神經保護、神經再生、促進血管新生及髓鞘修復等機制,顯著改善腦癱患者的運動功能、認知能力及生活質量。
然而,MSCs治療腦癱的療效并非一成不變,其效果依賴于細胞劑量與給藥途徑的科學選擇。不同劑量的MSCs在體內的分布、歸巢效率及作用強度存在顯著差異;而靜脈注射、鞘內注射等不同給藥方式,則直接影響細胞到達靶器官(如大腦皮層、白質區域)的效率及治療的精準性。
本文將系統綜述近年關于不同細胞劑量與給藥途徑對間充質干細胞治療腦癱療效影響的研究進展,結合具體臨床試驗數據,深入探討其機制差異與應用前景,為未來優化治療方案提供科學依據。

間充質干細胞治療腦癱:不同劑量與給藥途徑會影響療效嗎?
一、細胞劑量:從安全性到療效的梯度探索
1.1 干細胞治療腦癱的劑量-效應關系
干細胞(如間充質干細胞、神經干細胞)的療效與劑量呈非線性關系:
- 閾值效應:需達到最低有效劑量才能激活修復機制;
- 飽和效應:超過臨界劑量后療效不再顯著提升,但不良反應風險增加;
- 個體差異:患兒年齡、體重及腦損傷程度影響最佳劑量窗口。
1.2 低劑量方案(≤20×106細胞/次)
2024年,波蘭醫科大學在行業期刊《干細胞評論和報告》上發表了一篇關于《臍帶間充質干細胞對腦癱兒童運動功能的影響:真實世界、同情使用研究的結果》的臨床研究成果。

本次研究納入了152例腦癱患兒讓他們接受最多兩個療程、每療程五次的接受人臍帶間充質干細胞(hUC-MSCs)治療,每次劑量按體重分為10×106至40×106細胞。
研究結果表明:
1.粗大運動功能測量(GMFM):所有患兒(n=152)的GMFM中位評分在基線至第5次隨訪(第四次干細胞注射后)顯著提升1.9分,且改善與年齡呈負相關。并且所有GMFM子領域(如姿勢控制、移動能力等)均觀察到統計學顯著改善。
2.功能性活動測試:
- 6分鐘步行測試(6MWT):26名符合測試條件的輕中度患兒(GMFCS I-II級)中,步行距離中位數增加75米,改善與GMFM變化相關。
- 計時起立行走測試(TUG):26名患兒中位完成時間縮短2秒,改善與年齡相關,但與癲癇或性別無關。
3.臨床總體印象(CGI)評估:
- 治療后,39.7%患兒獲得輕微改善到III級,35.8%無變化,18.5%改善至II級,5.3%顯著改善至I級,僅0.7%患兒病情惡化。
- 改善程度與基線GMFCS分級顯著相關,且GMFM評分變化與CGI結果呈負相關。
4.肌肉力量(洛維特測試):63名患兒中,臀大肌力量改善最顯著(5.2%患兒提升1級),股四頭肌和肱二頭肌力量改善有限(僅少數患兒提升1-2級),但肌肉群間力量改善呈中等相關性。
綜上所述,低劑量多次臍帶間充質干細胞治療顯著改善了腦癱患兒的運動功能(尤其在GMFM評分和功能性活動能力),且對重度患者(GMFCS V級)具有潛在療效。然而,個體反應差異顯著,年齡和基線功能水平是關鍵影響因素。盡管肌肉力量改善有限,但綜合結果提示干細胞療法為重度腦癱患兒提供了一種安全有效的干預選擇。
1.3 中高劑量組(≥30-40×106細胞/次)
2021年,伊朗德黑蘭醫科大學在行業期刊《干細胞研究與治療》上發表了一篇關于《臍帶組織間充質干細胞鞘內注射治療腦癱的臨床及影像學結果:一項隨機雙盲假手術對照臨床試驗》的臨床結果。

患有痙攣性腦性癱瘓的參與者(4-14 歲)按 1:1 的比例分配接受UCT-MSC或假手術。實驗組注射單劑量(2 × 107個)細胞。
經過12個月的UCT-MSC治療,實驗組在運動功能、日常生活能力及生活質量方面均顯著優于基線組和對照組:
- 運動功能方面,GMFM-66評分較基線組提升10.65分,較對照組差異達8.07分,且MAS痙攣評分降低1.0分,提示粗大運動能力和肌張力顯著改善;
- 日常生活能力顯著提升,PEDI總評分較基線提高8.53分,較對照組差異達6.87分;
- 生活質量中,CP-QoL量表顯示“社交互動”“活動參與”等領域的改善程度顯著優于對照組;
- 影像學驗證顯示,實驗組白質完整性顯著修復:皮質脊髓束(CST)和皮質投射纖維(PTR)的FA值分別增加0.032和0.024,MD值分別降低0.035×10?3和0.045×10?3,均顯著優于對照組。
研究證明,一次性注射大量臍帶干細胞(2×10?個)能顯著改善腦癱患兒的運動能力、生活自理能力和社交質量。12個月后,孩子走路、抓握等動作更靈活,日常活動更獨立,大腦影像也顯示受損區域明顯修復。
二、給藥途徑:精準遞送與療效優化
2.1 靜脈輸注(IV):便捷性優先的全身調節
作為最常用途徑,靜脈輸注的優勢在于操作簡單、可重復性強,適用于各年齡段患兒。其核心機制是MSC通過血液循環到達腦部,分泌VEGF促進腦血管新生,同時調節外周免疫細胞。
2018年,我國兩家三甲醫院聯合在行業期刊《細胞移植》上發表了一篇關于《一項針對腦癱兒童的隨機、安慰劑對照的臍帶血間充質干細胞輸注試驗》的臨床研究成果。

本次研究納入了54例腦癱患者。輸注組27例患者接受4次hUCB-MSC輸注(靜脈輸注,固定劑量5×107)和基礎康復治療,而對照組27例患者接受0.9%生理鹽水和基礎康復治療。
功能評估對比:兩組患者基線期GMFM-88總分占比及CFA總分均無統計學差異,表明基線狀態均衡可比。
GMFM-88評分動態變化
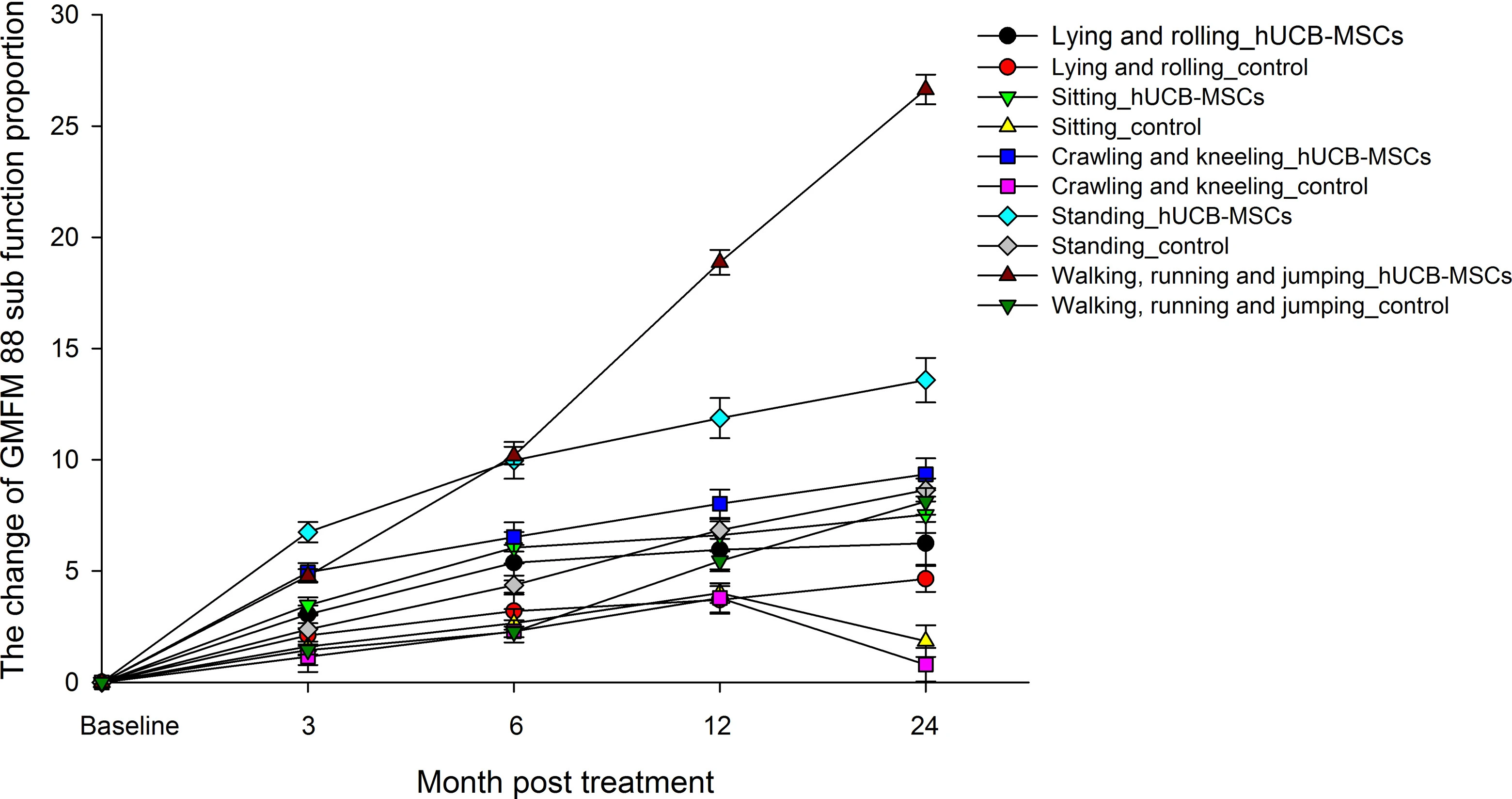
- 短期效果(3-6個月):hUCB-MSC組在治療后3個月即展現顯著改善,5個功能領域(坐位、爬行、跪位等)評分均呈上升趨勢;而對照組僅在治療后24個月出現輕微改善。
- 中長期效果(12-24個月):hUCB-MSC組在12個月時達到臨床有效標準,24個月時療效進一步鞏固,而對照組始終未達有效閾值。
- 統計學差異:hUCB-MSC組在治療后3、6、12、24個月的GMFM-88總分占比變化均顯著優于對照組,且各功能領域評分提升幅度持續擴大。(見圖1)
CFA評分動態變化
- 關鍵時間節點:hUCB-MSC組在治療后6個月首次達臨床有效,12個月維持有效,24個月進入顯著有效階段;對照組需至24個月才勉強達到有效下限。
- 功能領域改善:hUCB-MSC組各功能區CFA評分變化量均顯著高于對照組,尤其在運動協調、平衡能力等復雜動作領域優勢明顯。(見圖2)
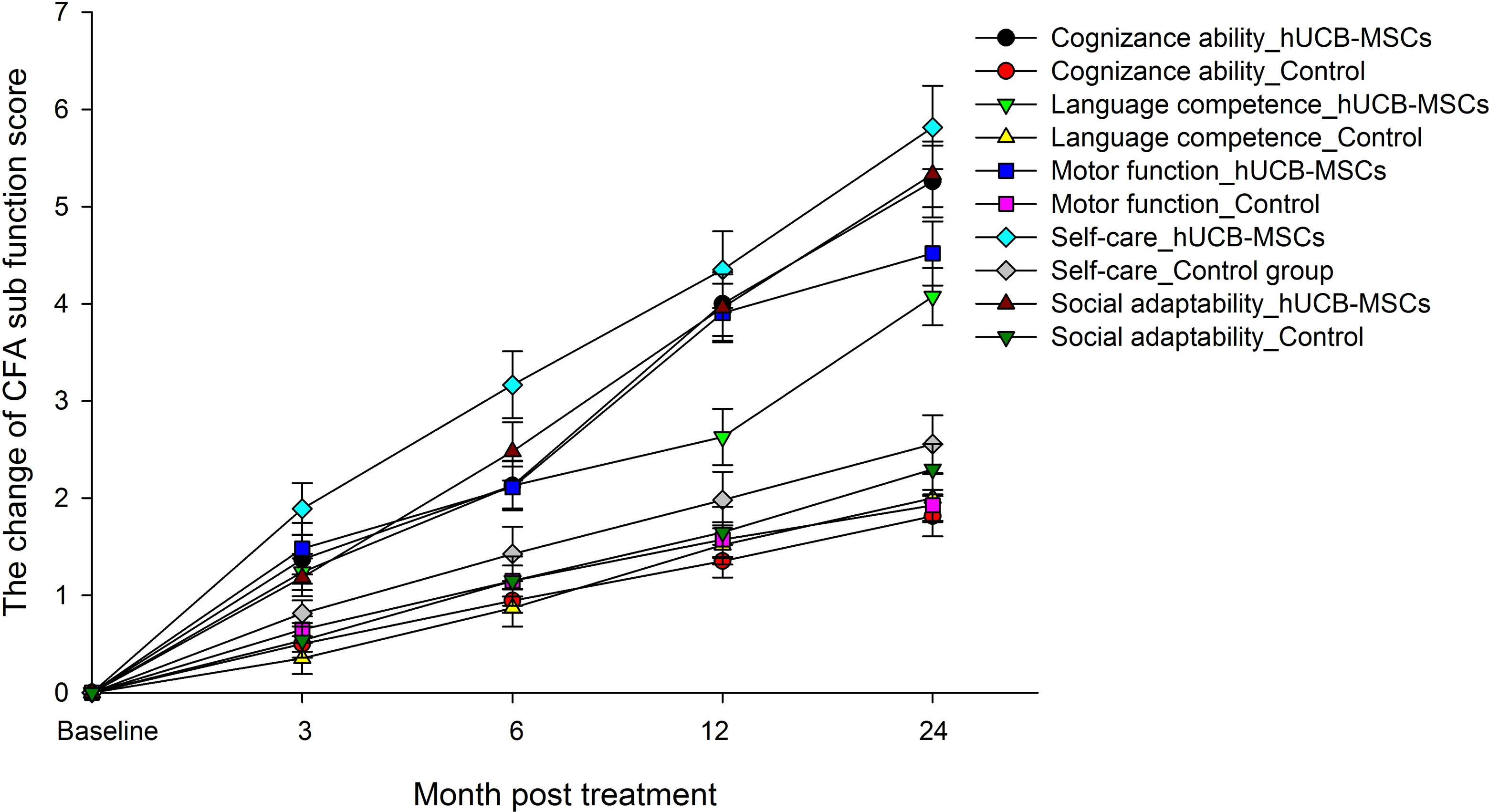
綜上所述,本研究證實人臍帶血間充質干細胞(hUCB-MSC)治療腦癱患兒具有顯著療效,在12-24個月內持續改善運動功能(GMFM-88)和精細動作能力(CFA),且效果優于常規治療。高細胞劑量與早期干預進一步放大療效,提示其通過調節神經電活動促進功能修復。
2.2 鞘內注射(IT):中樞靶向的強化效應
鞘內注射直接將MSC注入蛛網膜下腔,使細胞通過腦脊液循環富集于腦損傷區域,歸巢效率較靜脈途徑提高3-5倍。
2013年,武警總醫院曾在國際期刊《轉化醫學雜志》上發表了一篇關于《自體骨髓間充質干細胞來源的神經干細胞樣細胞用于治療腦癱患者》的臨床研究結果。

本次研究在鞘內注射(腰椎穿刺)前患者禁食禁水。采集骨髓前根據劑量和用法給患者注射苯巴比妥鈉、阿托品和氯胺酮。待患者睡著后,將局麻藥浸潤皮下,將脊椎穿刺針插入腰椎L3/L4或L4/L5之間,推進直至穿刺針穿過硬腦膜和薄蛛網膜進入蛛網膜下腔。
本研究于2010年6月至2011年6月入選60例運動功能嚴重受限的運動障礙型腦癱患兒,粗大運動功能分類系統平均Ⅲ-Ⅴ級。
經6個月隨訪,臍帶間充質干細胞移植組在粗大運動功能改善方面呈現顯著療效:
- 運動功能提升:治療后3個月,粗大運動功能測量評分較基線顯著提高42.6分;6個月時進一步增至58.6分,均顯著優于對照組。
- 語言功能:兩組在治療后1、3、6個月的語言商評分均未見顯著提升。
- 安全性:全部60名患者存活,且無嚴重不良事件或治療相關并發癥發生,證實該療法的安全性。
研究表明,臍帶間充質干細胞鞘內注射移植治療可顯著改善運動障礙型腦癱腦癱患兒的粗大運動功能,且在6個月內未觀察到嚴重不良反應,為該療法的臨床應用提供了有效性和安全性的支持證據。
2.3 腦內移植(IC):精準修復的爭議性探索
立體定向腦內移植可將MSC直接植入基底節、前額葉等受損腦區,在動物實驗中顯示神經元再生效率提升40%,但臨床應用仍限于少數難治性病例。
山東泰安市中心醫院曾在《中華醫學會第二十次全國物理醫學與康復學學術會議》上發表了一項《間充質干細胞移植治療小兒腦癱1:1配對病例對照分析》的臨床試驗。分析和總結應用骨髓間充質干細胞對腦癱患兒的運動功能療效。

本次研究隨機篩選適合進行干細胞移植的腦癱患兒15例作為移植組,同時選擇年齡、性別及疾病嚴重程度相仿的15例腦癱患兒為對照組。移植組采用微創定向手術進行直接顱腦穿刺注射。
研究結果表明,骨髓間充質干細胞移植治療后,術后1個月、3個月、1年移植組腦癱患兒的粗大運動功能、肌張力等粗大運動能力較對照組均得到不同程度提高。
三、劑量與途徑的總結
綜上所述,單一的細胞劑量或給藥途徑難以滿足所有腦癱患兒的治療需求,將不同劑量與給藥途徑相結合,并根據患兒的年齡、疾病嚴重程度、合并癥及個體反應差異制定個性化治療方案,成為未來發展的關鍵方向。
劑量方面,中高劑量可顯著改善重度腦癱患兒的運動功能和白質完整性,且療效持續時間較長;低劑量短期見效快,但需多次注射以維持療效,并可能通過增強神經可塑性實現長期功能鞏固。
給藥途徑中,靜脈輸注操作便捷、全身調節優勢顯著,但歸巢效率較低,適合輕中度腦癱或需全身免疫調節的患者;鞘內注射通過腦脊液循環富集于腦損傷區域,歸巢效率較靜脈途徑提高3-5倍,適合靶向修復;腦內移植通過微創定向手術實現精準修復,但存在侵入性操作風險,需嚴格評估適應癥。
綜合來看,高劑量+腦內移植適合重度腦癱或白質損傷顯著的患兒,以最大化局部修復效應;低劑量+靜脈輸注適合輕中度腦癱或需長期功能鞏固的患兒,兼顧安全性與便捷性;鞘內注射則為痙攣性腦癱或需快速靶向干預的患兒提供新方向,未來可結合影像導航技術優化精準性。
四、挑戰與未來方向
精準醫療:結合基因檢測和影像學技術,制定個性化劑量和給藥方案。
技術優化:開發新型生物材料和遞送系統,提高MSCs的靶向性和存活率。
政策支持:推動MSCs治療CP的臨床指南和監管框架,加速藥物審批進程。
結語
MSCs治療腦癱的潛力已通過多項臨床試驗驗證,但其療效高度依賴于細胞劑量和給藥途徑的選擇。未來需通過多中心研究進一步優化治療參數,推動標準化和個體化醫療的結合,最終實現從“實驗室突破”到“臨床治愈”的跨越。
相關閱讀:間充質干細胞治療腦癱安全嗎?22例患者5年隨訪揭示長期安全性
參考資料:
Chro?cińska-Kawczyk, M., Zdolińska-Malinowska, I. & Boruczkowski, D. The Impact of Umbilical Cord Mesenchymal Stem Cells on Motor Function in Children with Cerebral Palsy: Results of a Real-world, Compassionate use Study.?Stem Cell Rev and Rep?20, 1636–1649 (2024). https://doi.org/10.1007/s12015-024-10742-2
Amanat, M., Majmaa, A., Zarrabi, M.?et al.?Clinical and imaging outcomes after intrathecal injection of umbilical cord tissue mesenchymal stem cells in cerebral palsy: a randomized double-blind sham-controlled clinical trial.?Stem Cell Res Ther?12, 439 (2021). https://doi.org/10.1186/s13287-021-02513-4
Huang L, Zhang C, Gu J, et al. A Randomized, Placebo-Controlled Trial of Human Umbilical Cord Blood Mesenchymal Stem Cell Infusion for Children With Cerebral Palsy. Cell Transplantation. 2018;27(2):325-334. doi:10.1177/0963689717729379
Chen, G., Wang, Y., Xu, Z.?et al.?Neural stem cell-like cells derived from autologous bone mesenchymal stem cells for the treatment of patients with cerebral palsy.?J Transl Med?11, 21 (2013). https://doi.org/10.1186/1479-5876-11-21
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信